какой иммунитет формируется после введения иммуноглобулинов
Внутривенные иммуноглобулины, что и когда?
В настоящее время одну из ведущих позиций среди всех иммунобиологических лекарственных средств, зарегистрированных и разрешенных к применению у детей, занимают иммуноглобулины. Опыт использования антител в составе лечебных сывороток для профилактики и лечения инфекционных заболеваний насчитывает более чем 100-летнюю историю. В то же время практическое применение непосредственно иммуноглобулинов стало возможным только в 50-е годы ХХ столетия после разработки E.J.Kohn (1952) метода спиртового фракционирования плазмы крови. Благодаря этому открытию появилась возможность не только выделять в чистом виде и в большом количестве гамма-глобулины из нормальной плазмы, но и готовить из них лечебные препараты, содержащие антитела в высокой концентрации. Вначале иммунобиологической фарминдустрией был налажен выпуск иммуноглобулинов для внутримышечного введения (ИГВМ). ИГВМ характеризуется низкой скоростью поступления молекул иммуноглобулина в системный кровоток и существенным уровнем их разрушения в месте введения (Martin Du Pan R., 1959). Предпринимавшиеся попытки внутривенного введения препаратов иммуноглобулина для внутримышечного введения оказались крайне неудачными, т.к. сопровождались выраженными побочными эффектами. В дальнейшем было показано, что серьезные побочные эффекты при внутривенном введении ИГВМ обусловлены мощной стимуляцией системы комплемента агрегатами, состоящими из молекул иммуноглобулина. Оказалось, что в процессе производства ИГВМ происходит активация Fc-фрагмента иммуноглобулина, что приводит к образованию иммуноглобулиновых агрегатов. Только после разработки и внедрения в практику специальных методов обработки плазмы, препятствующих активации Fc-фрагмента молекулы антитела, появилась возможность производства безопасных препаратов иммуноглобулина для внутривенного введения (H.E.Schultze, G.Schwick, 1962; S.Barandum et al.,1962). В 70-80 годы внедрены технологии, позволившие создать внутривенные иммуноглобулины (ВВИГ), открывшие новую эру в лечении иммунной недостаточности и аутоиммунных заболеваний. (1,2,3).
Недостаточность иммуноглобулинов, и связанные с этим нарушения противоинфекционной резистентности возникают при первичных (генетически детерминированных) иммунодефицитах и вторичных иммунодефицитах, возникающих при воздействии неблагоприятных факторов на организм. Такими неблагоприятными факторами могут быть химио- и радиотерапия злокачественных новообразований, иммуносупрессивная терапия в трансплантологии, потеря белков плазмы и иммунокомпетентных клеток при кровопотерях, операциях, ожоговой болезни; воздействие эндотоксинов при некоторых инфекционных и паразитарных заболеваниях (4,5,6)
Другими областями применения ВВИГ являются лечение и профилактика определенных вирусных инфекций и лечение аутоиммунных заболеваний [7,8,9].
Существует много различных статей и монографий по применению иммуноглобулинов для внутривенного введения в различных областях медицины. Однако постоянно дискутируются три главных вопроса:
Для того чтобы ответить на эти вопросы, необходимо определиться с классификацией иммуноглобулинов, представленных на Российском рынке. Для практических целей может быть использована классификация ИГВВ, в основу которой положена особенность антительного состава препаратов. Принято выделять следующие группы ИГВВ:
У иммунобиологических препаратов производственный процесс влияет на качество. Поэтому так важно определиться в выборе препарата при рассмотрении клинической ситуации и быть уверенным в его эффективности и безопасности.
Вирусная безопасность препарата ВВИГ обеспечивается вирусной безопасностью плазмы и совершенством технологии производства. Контроль плазмы осуществляется при обследовании доноров в донорских центрах, карантинизацией с обязательным контрольным обследованием доноров в этот период. В процессе производства обязательна вирусная очистка и вирусная инактивация. Вирусная очистка включает:
В противоположность здоровым людям, у которых парвовирусная инфекция манифестирует в виде инфекционной эритемы или полиартропатии, у пациентов группы риска парвовирус В19 может вызвать серьезные нарушения кровообразования, в особенности эритропоэза.
У пациентов с врожденной и/или приобретенной гемолитической анемией или другими заболеваниями, сопровождающимися т.н. «эритропоэтическим стрессом», например, при железодефицитах, кровотечениях, после трансплантации почек или стволовых клеток, инфицирование парвовирусом В 19 может вызвать требующий срочной терапии «временный апластический криз». Он характеризуется утяжелением хронической анемии или на фоне компенсированного гемолиза внезапным появлением анемии с ретикулоцитопенией, сильным снижением или отсутствием эритроидных клеток-предшественников наряду с обнаружением проэритробластов в костном мозге, а также возможно сопровождается нейтропенией и тромбоцитопенией.
В группу риска входят также иммунокомпрометированные пациенты, так как вследствие нарушений гуморального иммунитета и недостаточной способности к элиминации вируса может возникнуть персистирующая инфекция с хронически протекающей парциальной красноклеточной аплазией костного мозга. Это касается пациентов с врожденным или приобретенным иммунодефицитом, пациентов с лимфопролиферативными заболеваниями во время/после химиотерапии и пациентов с ятрогенной иммуносупрессией (например, после высокодозовой химиотерапии и трансплантации стволовых клеток, вследствие аутоиммунных заболеваний, после трансплантации органов). Специфической противовирусной терапии не существует. В этом случае приходится прерывать терапию иммунодепрессантами или цитостатиками. В качестве методов лечения следует применять иммуноглобулины, предварительно убедившись, что они сами не контаминированы парвовирусом (так как обычные методы вирусинактивации не являются эффективными) и имеют специфические антитела против парвовируса.
Помимо хронической анемии у пациентов после аллогенной и аутологичной ТКМ было отмечено поражение парвовирусом внутренних органов. Так, у нескольких пациентов с кожной экзантемой при помощи ПЦР вирус был обнаружен не только в крови, но и частично в коже, у пациента с кардимиопатией – в миокарде, у пациента с гепатитом – в печени, а у пациента с гемолитико-уремическим синдромом – в почке. Летальность, ассоциированная с парвовирусной инфекцией, в данной группе пациентов составила 7%. Поэтому у иммунокомпрометированных пациентов с невыясненной причиной органной недостаточности следует исключать паровирусную инфекцию при помощи ПЦР из биопсийного материала.
Исходя из вышеизложенного, в терапии иммуноглобулинами пациентов из группы риска следует использовать только препараты, абсолютно безопасные с точки зрения передачи парвовируса В19.
В настоящее время только включение в производственный процесс нанофильтрации на фильтрах 20 нм приводит к полноценной элиминации парвовируса В19 (рис. 1). Все остальные способы вирусинактивации лишь ограниченно способны инактивировать данный вирус. Это отмечено в инструкции по применению, например, препарата Октагам. По открытым данным о производстве препаратов, иммуноглобулины Имбио и Габриглобин проходят только одну стадию вирусной инактивации, данных об элиминации парвовируса В19 нет. В настоящее время в РФ зарегистрирован препарат иммуноглобулина человека Интратект, в процесс производства которого наряду с традиционными стадиями инактивации / элиминации вирусов также включена нанофильтрация.
Эффективность и переносимость ВВИГ обеспечивается:
Основные показания к применению стандартных иммуноглобулинов:
1. Профилактика или заместительная терапия.
Механизм действия заместительной терапии заключается в связывании и нейтрализация микробного антигена, блокировании присоединения вирусов и бактерий к клетке-мишени, опсонизации и инициация поглощения и переваривания вирусов и бактерий фагоцитами, наличием нейтрализующих антител против суперантигенов. Стандартными дозами ВВИГ для заместительной терапии являются 400-500 мг/кг массы тела пациента 1 раз в 3-4 недели (период полураспада IgG). Необходимо обратить внимание на то, чтобы претрансфузионный уровень сывороточного IgG был не менее 4-5 г/л. Хорошее состояние и нормальный претрансфузионный уровень IgG не являются показанием для уменьшения дозы вводимого ВВИГ и/или увеличения интервалов между трансфузиями. Для заместительной терапии используют только препараты стандартных иммуноглобулинов (11, 12). Применение Пентаглобина нерационально и может вызвать серьезные побочные реакции в связи активацией комплемента и образованием IgM содержащих иммунных комплексов (13, 14). Кому же применяется заместительная терапия?
2. Терапия аутоиммунных заболеваний.
Эффект высокодозовой терапии (1-2 г/кг массы тела пациента в течение последовательных 2-3 дней) обеспечивается следующими механизмами (15, 16, 17, 18):
Препаратами первой линии терапии ВВИГ являются при:
Высокодозовая терапия ВВИГ используется также при:
Рассеянном склерозе, миастении гравис, воспалительных миозитах, системных васкулитах, аутоиммунных цитопениях при системной красной волчанке, аутоиммунных дерматитах, в профилактике спонтанных абортов (лечение антифосфолипидного синдрома), аутоиммунных цитопениях (аутоиммунная нейтропения, аутоиммунная гемолитическая анемия, аллоиммунной неонатальной тромбоцитопении и гемолитической анемии) (19, 20).
За 30 лет применения ВВИГ проведено много рандомизированных, контролируемых исследований, которые достоверно доказали снижение частоты и интенсивности инфекционных осложнений при проведении ежемесячной терапии иммуноглобулином IgG в дозе 250-500 мкг/кг массы тела (21, 22, 23).
Вторая группа – поликлональных ВВИГ, обогащенных IgM и IgA, представлена единственным препаратом, не имеющим аналогов, под торговым названием Пентаглобин. Состав препарата: Ig G = 76%, Ig M = 12% и Ig А=12 %.
Все положительные эффекты данного препарата связаны именно с наличием в их структуре иммуноглобулина М и иммуноглобулина А.
Пентаглобин разработан для лечения распространенных тяжелых бактериальных инфекций за счет специфических функций, которыми обладают иммуноглобулины классов А и М.
Основным показанием к клиническому применению Пентаглобина является адъювантная терапия бактериальных инфекций. Преимущество Пентаглобина перед стандартными ВВИГ в терапии сепсиса доказано многочисленными клиническими исследованиями. Вначале проводились оригинальные, рандомизированные клинические исследования, а с 2001 года начали проводиться мета-анализы для получения более достоверных с точки зрения статистики данных, которые объединяют качественные клинические исследования и оценивают эффективность адъювантной терапии иммуноглобулинами. Все они показали преимущества Пентаглобина и подтверждены международными экспертами 25. Один из ведущих специалистов в области интенсивной терапии профессор Werdan K в 2007 году провел мультицентровое исследование SBITS (30) с целью доказательства эффективности применения стандартных иммуноглобулинов (IgG) в лечении сепсиса у взрослых больных. Протокол был опубликован до начала исследования и послужил основой для последующей дискуссии о методологии клинических исследований по сепсису. Результаты работы были опубликованы в одном из самых авторитетных журналов по интенсивной терапии Critical Care Medicine. В группу IgG было включено 321 пациент, в контрольной группе (плацебо альбумин) было 303 больных.
Летальность в группе IgG составила 39,3%, а группе альбумина 37,3%.
Ожидания исследователей не оправдались: у взрослых пациентов с сепсисом не произошло статистически достоверного снижения летальности. Авторы сделали вывод, что стандартные иммуноглобулины IgG не должны использоваться в качестве адъювантной терапии сепсиса.
По мнению международных экспертов, это исследование превосходит все проведенные прежде исследования как по качеству, так и по числу включенных пациентов, и должно рассматриваться как знаковое в этой области.
Таким образом, пентаглобин является первым и единственным препаратом, который воплощает естественные, природные принципы физиологической защиты организма человека:
Терапия Пентаглобином является «золотым стандартом» лечения сепсиса и септического шока.
Режим дозирования: лечение активной инфекции 1 – 2 мл на кг массы тела каждые 48 часов 3 – 5 введений или до исчезновения клинических симптомов; профилактика реактивации – 1 мл/кг массы тела 1 раз в триместр у беременных или 6 раз с интервалом 3-4 недели после трансплантации. Необходимо отметить, что использование иммуноглобулинов совместно с виростатическими препаратами дает лучшие результаты (33).
Применение Неоцитотекта предотвращает развитие вирус-индуцированной лимфопролиферации (34). Результаты ретроспективного анализа более чем 26000 пациентов с трансплантированной почкой выявили стандартизированную частота развития опухоли в 1-й год после операции:
Неогепатект применятся для профилактики заражения гепатитом В одновременно с вакцинацией у новорожденных, родившихся от матерей вирусоносителей, пациентов, получающих терапию гемодиализом, пациентов, получающих множественные гемотрансфузии; у невакцинированных лиц, при контакте с кровью больного (35, 36, 37, 38, 39, 40). Также Неогепатект вводится лицам, не ответившим на предшествующую вакцинацию при риске заражения. Режим дозирования:
Как в организме вырабатываются антитела после вакцины?
У моих пациентов возникает много вопросов по поводу вакцинации. Основные – как работает иммунитет и как в ответ на вакцину вырабатывается иммунная защита, откуда берутся антитела. Разберемся в этом вопросе.
Иммунная система и иммунизация
Иммунизация предотвращает заболевание, позволяя организму быстрее реагировать на нападение и усиливая иммунный ответ на конкретный организм.
Как организм понимает, что вторглись чужие?
Каждый патоген имеет уникальные отличительные компоненты, известные как антигены, которые позволяют иммунной системе различать «я» (тело) и «чужое» (чужеродный материал).
Когда иммунная система впервые видит новый антиген, она должна подготовиться к его уничтожению. За это время возбудитель может размножиться и вызвать болезнь.
Однако, если тот же самый антиген обнаруживается снова, иммунная система готова ограничить и быстро уничтожить организм. Это адаптивный (специфический, приобретенный) иммунитет.
Вакцины используют этот адаптивный иммунитет и память, чтобы подвергнуть организм действию антигена, не вызывая заболевания. Поэтому, когда живой патоген поражает организм, реакция происходит быстро, и патоген не может вызвать болезнь.
В зависимости от типа инфекционного организма, реакция, необходимая для его удаления, различается. Например, вирусы скрываются в собственных клетках организма в различных тканях, таких как: горло, печень и нервная система, и бактерии могут быстро размножаться в инфицированных тканях.
Линии защиты организма
Слизистые
Внутренние защитные силы организма
Иммунный ответ
Иммунный ответ срабатывает, когда иммунная система получает предупреждение о проникновении в организм чего-то постороннего.
Триггеры включают выброс химических веществ поврежденными клетками и воспаление, а также изменения в кровоснабжении поврежденной области, которые привлекают лейкоциты.
Белые кровяные тельца уничтожают инфекцию или передают химические сообщения другим частям иммунной системы. Поскольку кровь и тканевые жидкости циркулируют по телу, различные компоненты иммунной системы постоянно исследуют потенциальные источники атаки или аномальные клетки.
Антигены и антитела
Антигены обычно представляют собой белки или полисахариды (длинные цепи молекул сахара, которые составляют клеточную стенку определенных бактерий).
Их название происходит от «генераторы антител». Любой конкретный организм содержит несколько разных антигенов.
Первоначально иммунный ответ включает выработку антител, которые могут связываться с определенным антигеном, и активацию антиген-специфических лейкоцитов.
Классы антител
Обычно в жидкостях тканей тела циркулируют низкие уровни антител. Тем не менее, когда активируется иммунный ответ, вырабатывается большее количество, специфически нацеленное на чужеродный материал.
Вакцинация увеличивает уровень циркулирующих антител против определенного антигена. Антитела вырабатываются лейкоцитами (лимфоцитами), которые называются В-клетками. Каждая В-клетка может продуцировать антитела только против одного специфического эпитопа.
При активации В-клетка будет размножаться, чтобы производить больше клонов, способных секретировать это конкретное антитело. Класс продуцируемых антител определяется другими клетками иммунной системы, это известно как клеточно-опосредованный иммунитет.
Первичный ответ
При контакте с патогеном тело попытается изолировать и уничтожить его.
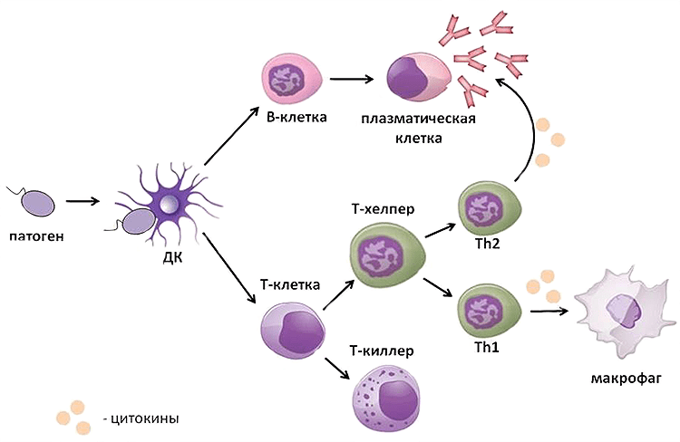
Химические вещества, выделяемые при воспалении, увеличивают кровоток и привлекают лейкоциты в область инфекции. Специализированные клетки, известные как фагоциты, поглощают цель и разбирают ее.
Затем эти фагоциты перемещаются к ближайшим лимфатическим узлам, где они «представляют» антигены другим клеткам иммунной системы, чтобы вызвать более крупный и более специфический ответ. Этот ответ приводит к выработке антиген-специфических антител.
Затем циркулирующие антитела находят организм и связываются с его поверхностными антигенами. Таким образом, он помечается как цель. Этот специфический ответ также называется адаптивным или клеточно-опосредованным иммунным ответом, поскольку иммунная система адаптируется к типу захватчика.
Когда организм впервые подвергается воздействию антигена, проходит несколько дней, прежде чем этот адаптивный ответ становится активным. При первом контакте с патогеном иммунная активность увеличивается, затем выравнивается и падает. Поскольку первый, или первичный, иммунный ответ является медленным, он не может предотвратить заболевание, хотя может помочь в выздоровлении.
Как только антиген-специфические Т- и В-клетки (лимфоциты) активируются, их количество увеличивается, и после заражения некоторые клетки памяти остаются, что приводит к памяти на специфические антигены. Для полного развития этой памяти может потребоваться несколько месяцев.
Вторичный ответ
При последующих контактах с одним и тем же патогеном, иммунная система способна быстро реагировать, и активность достигает более высокого уровня.
Вторичные иммунные реакции обычно могут предотвратить заболевание, поскольку патоген обнаруживается, атакуется и уничтожается до появления симптомов.
В целом, взрослые реагируют на инфекцию быстрее, чем дети. Организм способен предотвратить заболевание или уменьшить его тяжесть за счет быстрого и сильного иммунного ответа на антигены, с которыми он столкнулся ранее.
Дети же не встречали столько антигенов и поэтому чаще болеют.
Некоторые инфекции, такие как ветряная оспа, вызывают память об инфекции на всю жизнь. Другие инфекции, такие как грипп, варьируются от сезона к сезону до такой степени, что даже взрослый человек не может адаптироваться.
Вакцинация
Вакцинация использует этот вторичный ответ, подвергая организм воздействию антигенов определенного патогена и активируя иммунную систему, не вызывая заболевания.
Первоначальный ответ на вакцину аналогичен первичному ответу при первом контакте с патогеном, но медленный и ограниченный. Последующие дозы вакцины усиливают этот ответ, что приводит к выработке долгоживущих антител и клеток памяти, как это было бы естественно после последующих инфекций.
Вакцины различаются по тому, как они стимулируют иммунную систему.
Некоторые дают более широкий ответ, чем другие. Вакцины влияют на иммунный ответ через природу содержащихся в них антигенов, включая количество и характеристики антигенов, или через путь введения: пероральная, внутримышечная или подкожная инъекция.
Виды иммунизации
Антитела передаются от матери младенцу через плаценту и с грудным молоком, чтобы защитить младенцев в течение короткого времени после рождения.
Антитела (иммуноглобулины) также очищают из крови или в лабораториях; их можно вводить напрямую, чтобы обеспечить быструю, но непродолжительную защиту или лечение определенных заболеваний, таких как бешенство, дифтерия и столбняк.
John TJ, Samuel R. Herd immunity and herd effect: new insights and definitions. Eur J Epidemiol 2000; 16:601–6.
Иммунитет
Иммунная система осуществляет защиту организма от инфекционных и неинфекционных чужеродных агентов. При появлении и накоплении в организме клеток, отличающихся генетически, запускается каскад иммунных реакций и формируется иммунный ответ.
Основное назначение иммунной системы — это обезвреживание потенциально опасного антигена и формирование резистентности к нему.
Строение
Иммунная система состоит из совокупности лимфоидных органов и тканей, суммарная масса которых составляет 2% от массы тела и которые разрознены между собой в анатомическом смысле. Однако благодаря наличию медиаторов, сигнальных молекул и клеток, способных к миграции в различные органы и ткани, иммунная система представляет четко организованную структуру в функциональном смысле.
Иммунная система включает центральные и периферические органы. К центральным относят тимус и костный мозг. В этих органах начинается созревание зрелых лимфоцитов.
Периферические органы объединяют селезенку, лимфатические узлы и лимфоидную ткань, печень, кровь, лимфу. Наиболее известными структурами являются миндалины и пейеровы бляшки.
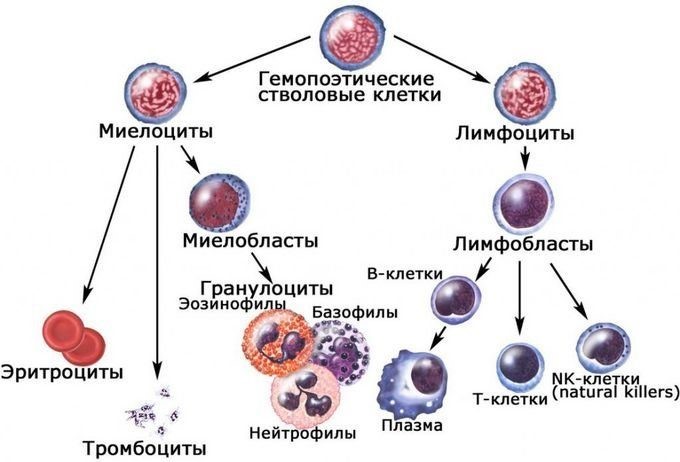
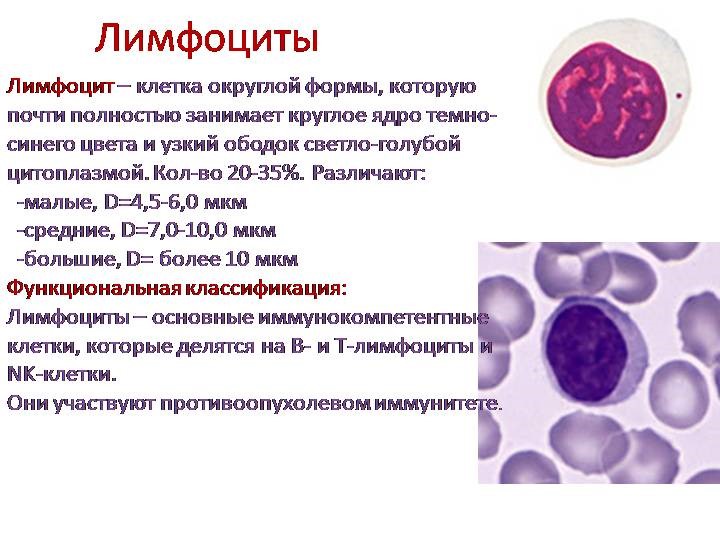
Лимфоциты — основные функциональные клетки иммунной системы. Они образуются в костном мозге, а затем проходят созревание. В зависимости от того, в каком органе лимфоциты проходят созревание, они подразделяются на две гетерогенные популяции: Т-лимфоциты (тимус) и В-лимфоциты (лимфоузлы). Т-лимфоциты ответственны за клеточный иммунитет, В-лимфоциты отвечают за гуморальный. В-лимфоциты являются предшественниками антителообразующих клеток.
Благодаря существованию механизма «иммунологической памяти», иммунный ответ при повторном взаимодействии с теми же антигенами возникает в более короткие сроки и имеет более яркое выражение. Индукция иммунитета является благоприятным исходом иммунных реакций и ведет к восстановлению гомеостаза организма.
Виды иммунитета
Состояние иммунитета обеспечивают наследуемые и индивидуально формируемые механизмы.
К первому относится невосприимчивость человека или определенных видов животных к возбудителям некоторых инфекционных болезней. Например, люди невосприимчивы к возбудителю чумы собак, многие животные — к вирусу кори, гонококку и т.д. Устойчивость к соответствующей инфекции наследуется, как видовой признак, и проявляется у всех представителей данного вида. Это врожденный иммунитет или видовой.
Приобретенный иммунитет формируется в течение всей жизни индивидуума. Примером естественного приобретенного иммунитета является невосприимчивость к инфекции после перенесенного заболевания. Так называемый постинфекционный иммунитет. Например, ветряная оспа.
Приобретенный иммунитет может быть активным и пассивным. Активно приобретенный иммунитет возникает в результате перенесенного инфекционного заболевания или введения в организм вакцины. Пассивно приобретенный иммунитет формируется при передаче антител от матери к плоду или может быть искусственно создан путем парентерального введения в организм готовых иммунореагентов. К ним относят специфические иммуноглобулины, иммунные сыворотки и лимфоциты, способные защитить организм от антигенов.
Иммунитет может быть генерализованным и местным. При местном иммунитете происходит защита покровов организма, которые контактируют с внешней средой: слизистые оболочки мочеполовых органов, желудочно-кишечного тракта и т.д.
Иммунный статус
Характеристику состояния иммунной системы организма, выраженную количественными и качественными показателями ее компонентов, называют иммунным статусом. Определение иммунного статуса проводят с целью правильной постановки диагноза заболевания, прогнозирования его течения и выбора метода лечения.
Иммунная система человека
к.м.н. Гольдинберг Б. М., Васюк Я.В.
Городской центр трансфузиологии учреждения здравоохранения «6-я городская клиническая больница», г. Минск,
учреждение здравоохранения «7-я городская детская поликлиника», г. Минск
ИММУНННАЯ СИСТЕМА ЧЕЛОВЕКА
Введение
Группа органов, имеющих общее происхождение, единый план строения и выполняющая общую функцию называется системой органов. Пять из всех десяти систем органов являются регулирующими (управляющими): нервная, кровеносная, эндокринная, лимфатическая и иммунная. Уточним, что лимфатические органы и лимфатических узлы, которых насчитывается около 600, функционально является частью иммунной системы, а к собственно лимфатической системе относится обширная сеть сосудов, которая проходит почти через все наши ткани, обеспечивая движение жидкости, называемой лимфой.
Слово «иммунитет» происходит от латинского «immunis» (на английском – immunity), что означает «чистый от чего-либо», невосприимчивый к чему-либо. Иммунная система появилась вместе с многоклеточными организмами и развивалась, как помощница их выживанию. Она объединяет органы и ткани, которые гарантируют защиту организма от генетически чужеродных клеток и веществ, поступающих из окружающей среды.
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным.
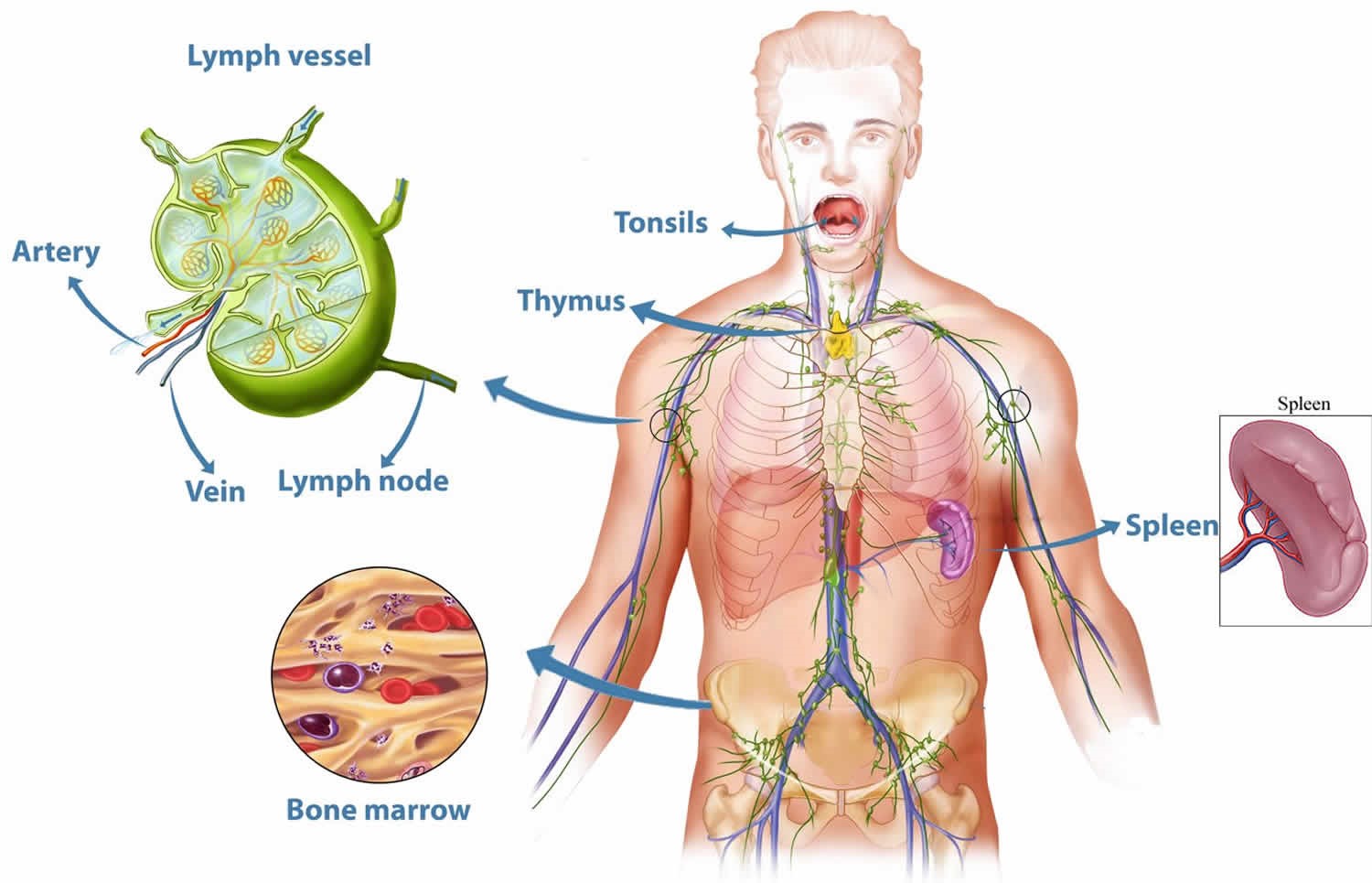
Органы иммунной системы человека
Иммунная система включает центральные и периферические органы.
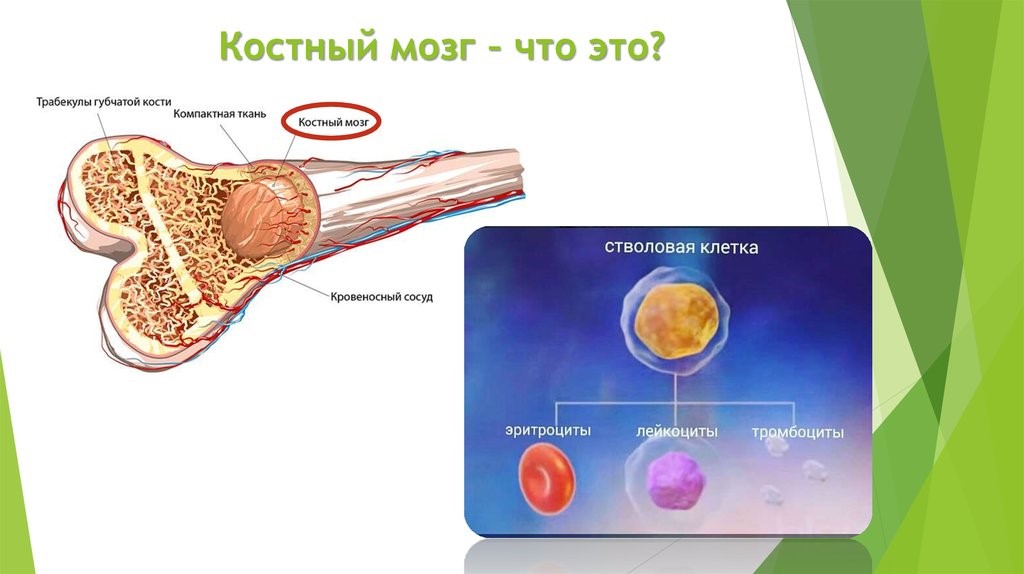
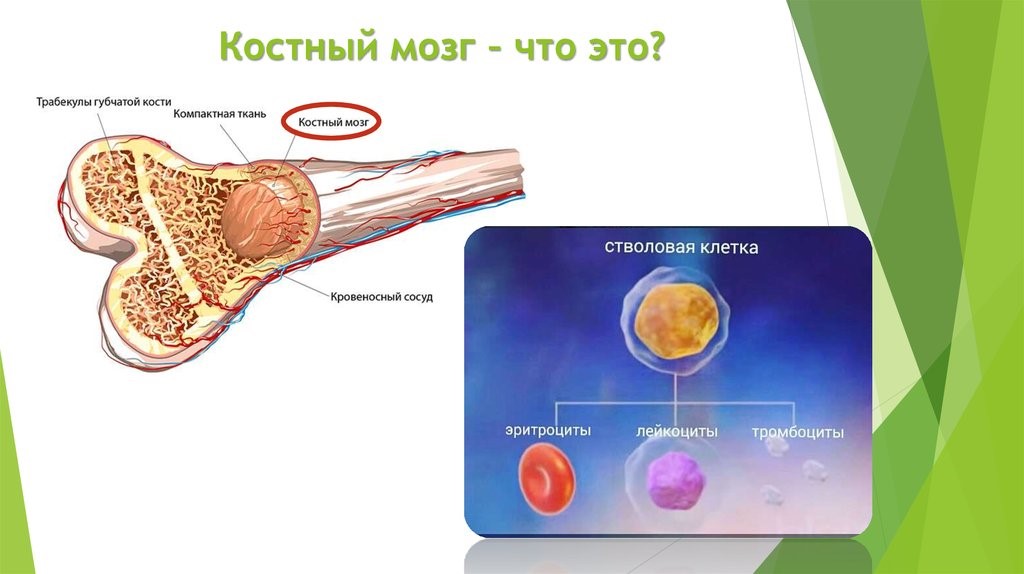
Центральные органы иммунной системы представляют собой красный костный мозг и тимус.
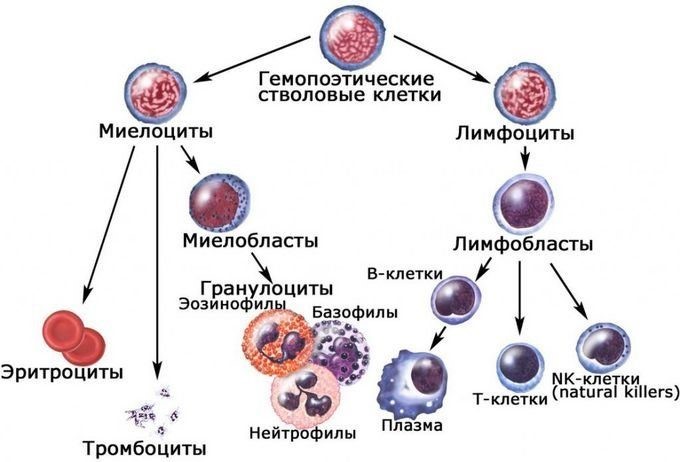
Костный мозг является хранилищем стволовых клеток, из которых образуются клетки крови (рис.1). В зависимости от ситуации, стволовые клетки трансформируются в иммунные В-лимфоциты. При необходимости, определенная часть B-лимфоцитов превращается в плазматические клетки, которые способны вырабатывать антитела.
Рис.1. Костный мозг содержит стволовые клетки
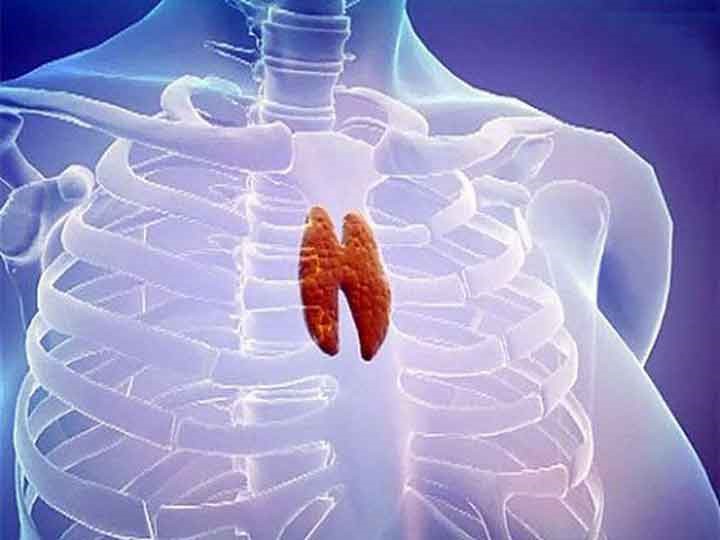
Тимус (или вилочковая железа) – один из главных органов иммунной системы, расположенный у человека за грудиной ниже ключиц, который отвечает за образование Т-клеток иммунной системы в лимфоидных тканях организма (рис.2).
К периферическим органам относятся селезенка, миндалины и лимфоузлы, в которых находятся зоны созревания иммунных клеток.
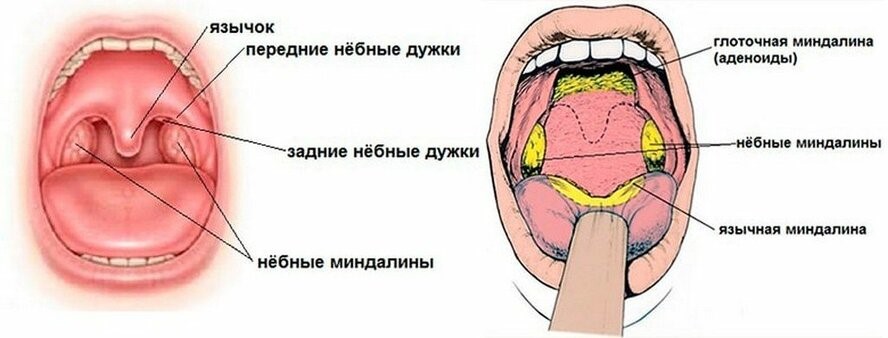
Миндалины, получившие свое название из-за внешней схожести с миндалем, представляют собой скопление лимфоидной ткани в верхней части носоглотки. У человека шесть миндалин: две небные, две грудные и по одной носоглоточной и язычной.
Самыми крупными из них являются небные миндалины, или гланды, которых легко осмотреть самостоятельно в зеркале, если достаточно широко раскрыть рот (рис.3).
Рис. 3. Небные миндалины
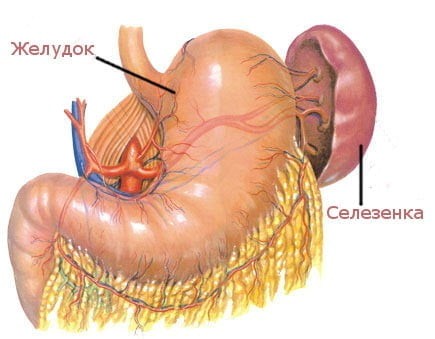
Селезенка является самым крупным лимфоидным органом (рис. 4). Кроме того, она может накапливать некоторое количество крови. В экстренных ситуациях селезенка способна послать свои запасы в общий кровоток. Это позволяет улучшить качество и скорость иммунных реакций организма. Селезенка очищает кровь от бактерий и перерабатывает всевозможные вредные вещества. В ней полностью разрушаются эндотоксины, а также остатки умерших клеток при ожогах, травмах или других повреждениях тканей. У людей, оставшихся по какой-либо причине без селезенки, ухудшается иммунитет.
Лимфатические узлы представляют собой небольшие образования округлой формы (рис. 5), расположенные в грудной полости (бронхолегочные, бронхотрахеальные) и брюшной полости (пейеровы бляшки, аппендикс и другие), окологрудные на поверхности грудной клетки, на шее и на конечностях. Лимфоузел – это один из барьеров на пути инфекций и раковых клеток, играющий роль своеобразной таможни (рис. 5). В нем образуются лимфоциты – специальные клетки, которые принимают активное участие в уничтожении вредных веществ.
Центральные органы иммунной системы отвечают за образование и созревание клеток, а периферические органы обеспечивают защиту, то есть иммунный ответ. Периферические и центральные органы иммунной системы выполняют свои работу только вместе и если выходит из строя какой-либо один из этих органов, то организм лишится защитного барьера.
Компоненты иммунной системы
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции (сущности).
Врожденный (видовой) иммунитет – наследственно закрепленная система защиты организма человека от патогенных и непатогенных микроорганизмов, а также продуктов тканевого распада. Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркёрам – так называемым «образам патогенности». Эти маркёры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с возмутителями спокойствия: чужаком или своим, но ставшим для организма предателем (рис.6).
Рис.6. Врожденный иммунитет: главное – спокойствие!
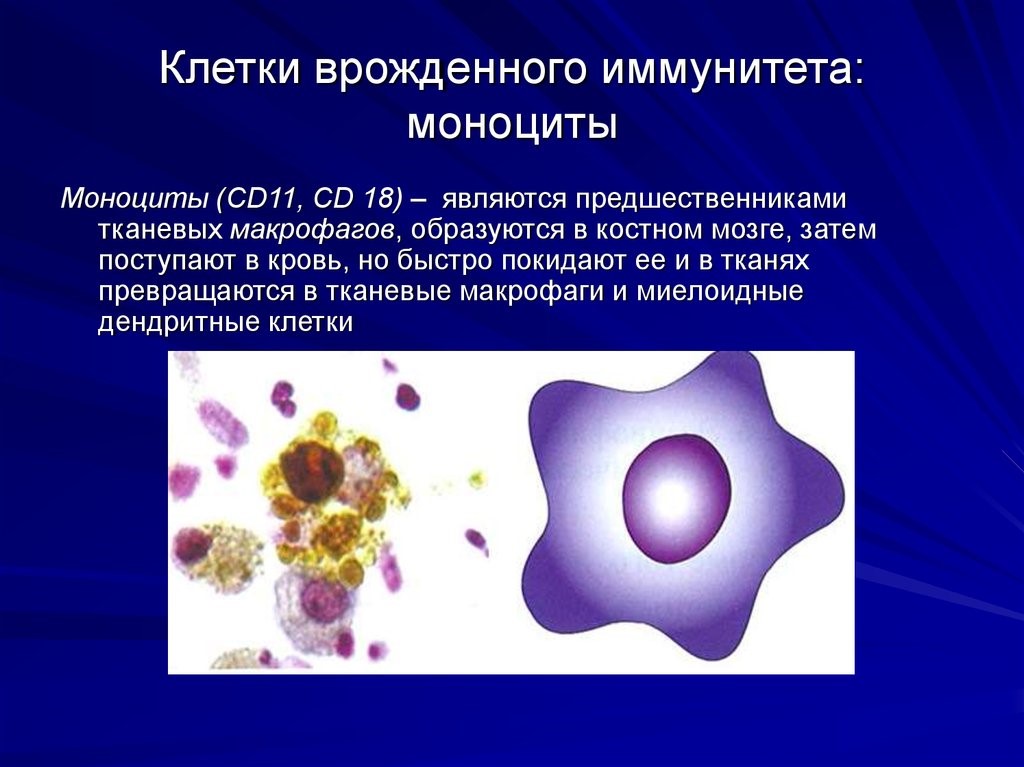
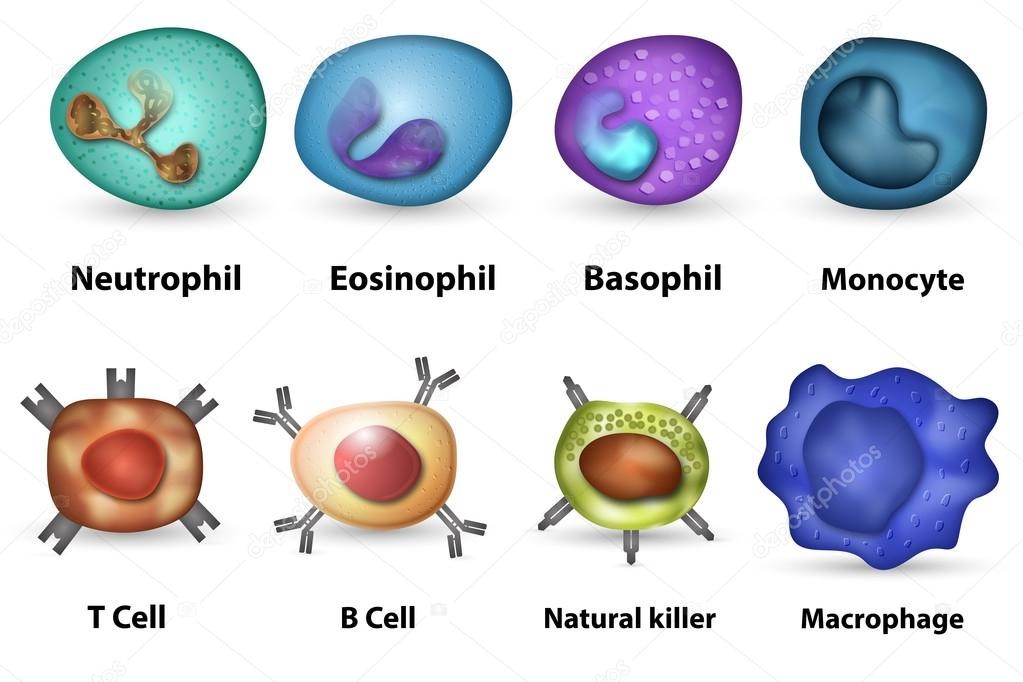
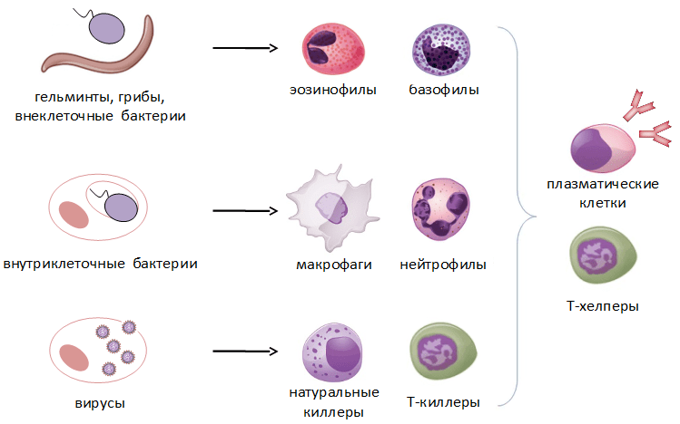
Врожденный иммунитет на клеточном уровне представляют:
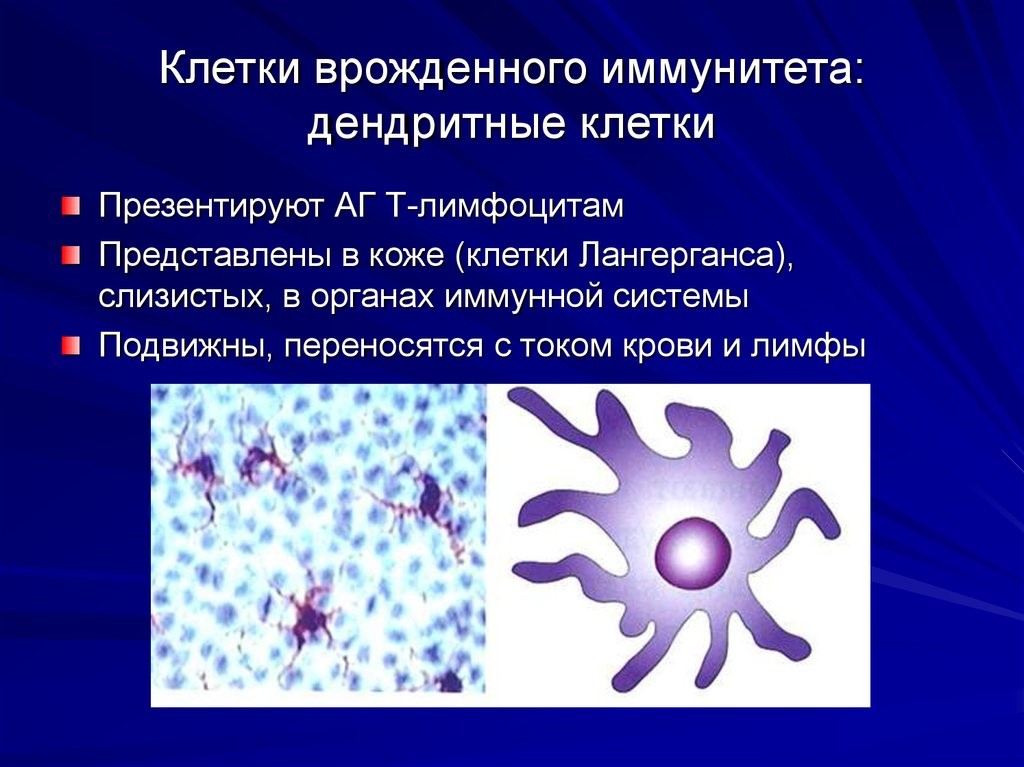
Рис.8. Дендритная клетка и
Нейтрофилы – самые многочисленные иммунные клетки в крови человека. Они циркулируют в крови всего 8-10 часов и бόльшую часть своей жизни путешествуют по тканям организма. При встрече с патогеном они его захватывают и переваривают, после чего обычно сами погибают. Из разрушенных нейтрофилов высвобождаются гранулы, содержащие антибиотические вещества.
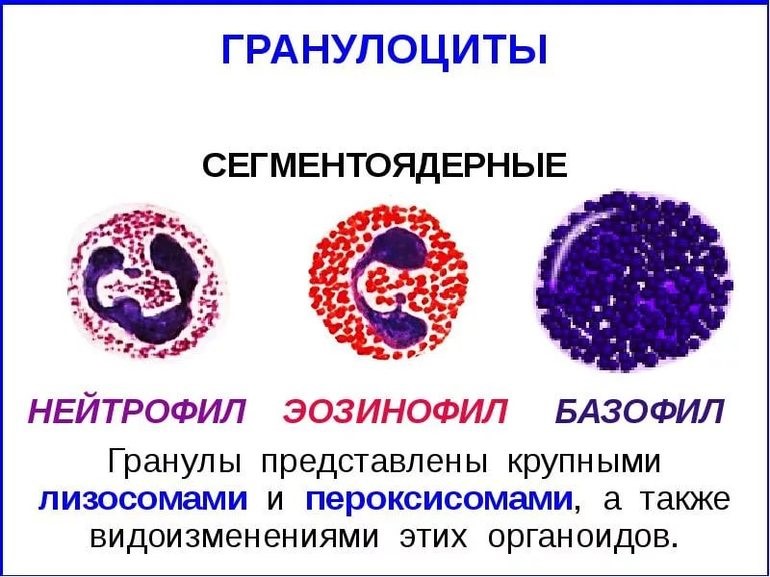
Гранулы эозинофилов и базофилов осуществляют химическую защиту организма от крупных патогенов, например, паразитических червей, грибов, внеклеточных бактерий. Однако при чрезмерной активности могут участвовать и в развитии аллергической реакции;
Рис.10. Натуральный киллер
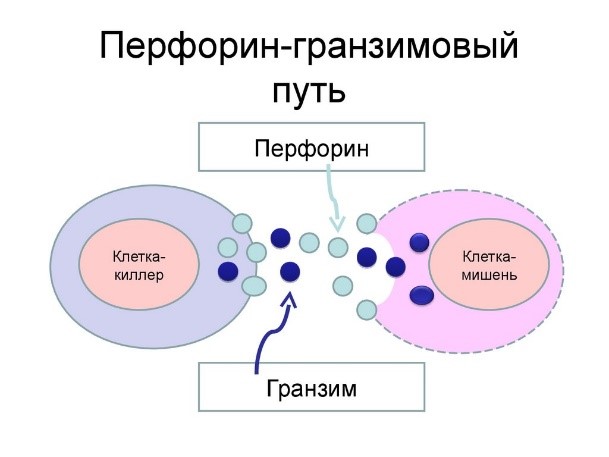
Действуют натуральные киллеры с помощью агрессивных веществ перфорина и гранзима, которые наподобие буравчиков «кусают» и разрушают пораженную клетку, ставшую для них мишенью (рис.11)
Рис.11. Проникновение перфорина и гранзима в раковую клетку и ее уничтожение
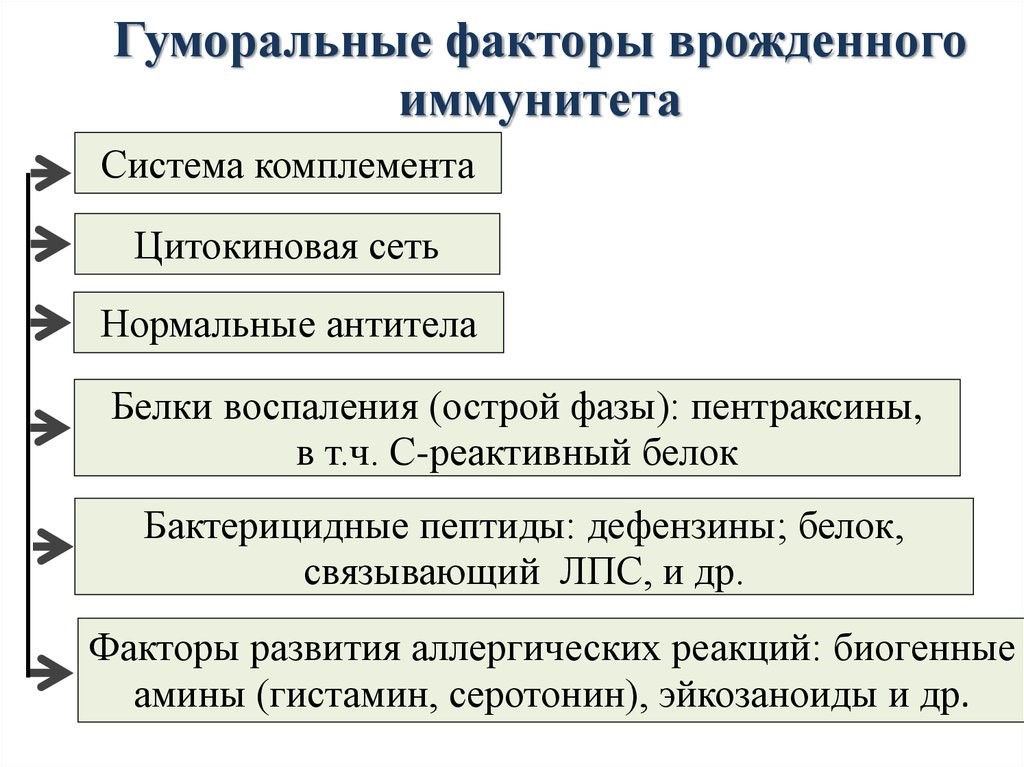
Молекулярными(гуморальные) факторами врожденного иммунитета являются (рис.12):
Рис.12.Гуморальные факторы врожденного иммунитета
Система комплемента – это многокомпонентная самособирающаяся система более 20 сывороточных белков, которые в норме находятся в неактивном состоянии.
После активации проявляются биологические эффекты комплемента: образование мембраноатакающего комплекса для лизиса патогенов, выброса медиаторов воспаления для привлечения фагоцитов и усиления их поглотительной способности.
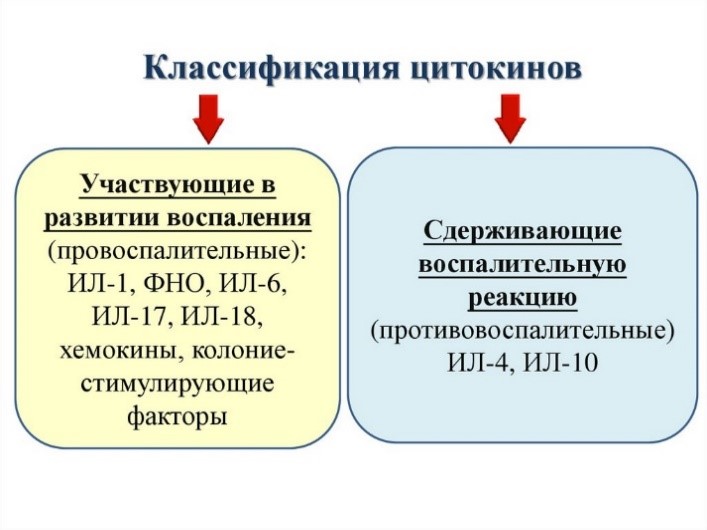
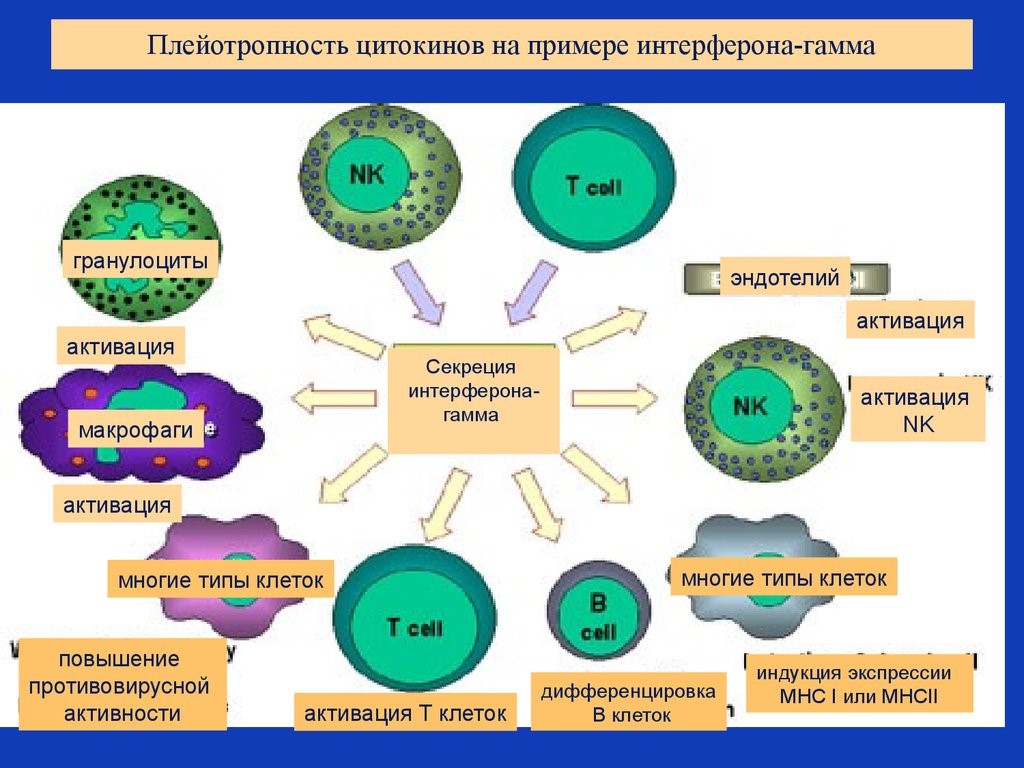
Цитокины – это система низкомолекулярных белков организма, синтезируемых преимущественно активными клетками иммунной и кроветворной систем, регулирующих межклеточные взаимодействия «универсальный» язык для всех клеток), представленные на рис.13 и 14.
Рис. 13. Цитокины: ИЛ – интерлейкины, которых в настоящее время насчитывается 34 разновидности;
Рис. 14. Разнонаправленность действия цитокинов на примере гамма-интерферона
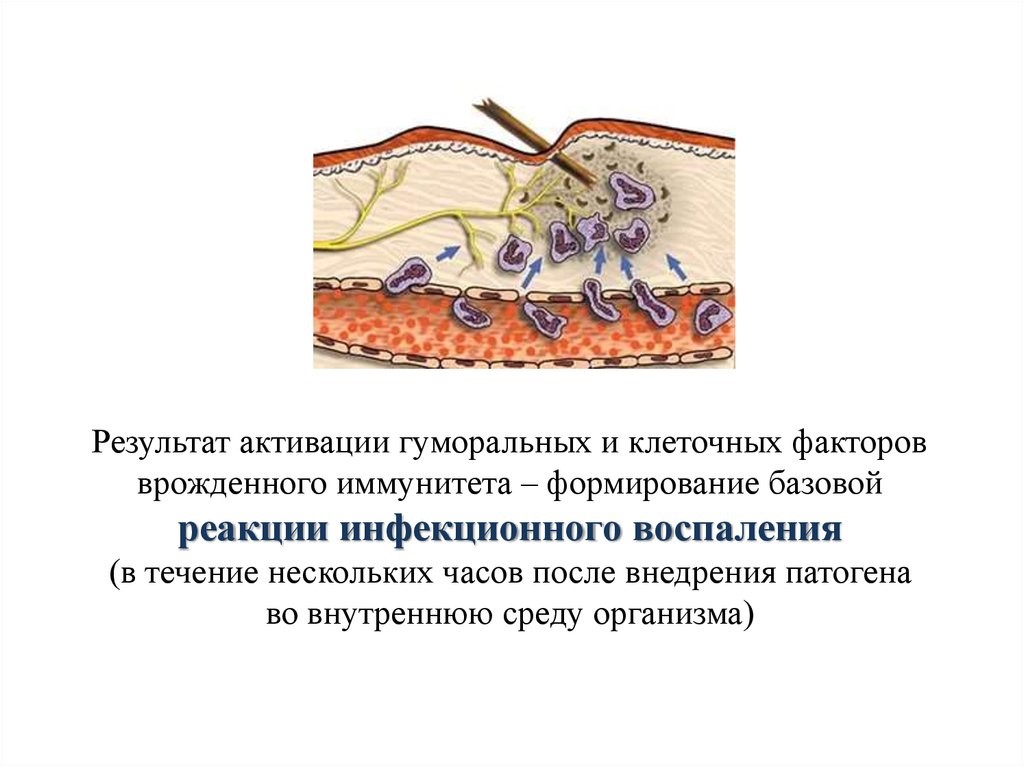
В результате активации гуморальных и клеточных факторов врожденного иммунитета в течение нескольких часов после внедрения патогена во внутреннюю среду организма формируется базовая реакция инфекционного воспаления (рис. 15)
Рис. 15. Инфекционное воспаление ткани на месте внедрения инородного тела с целью его удаления
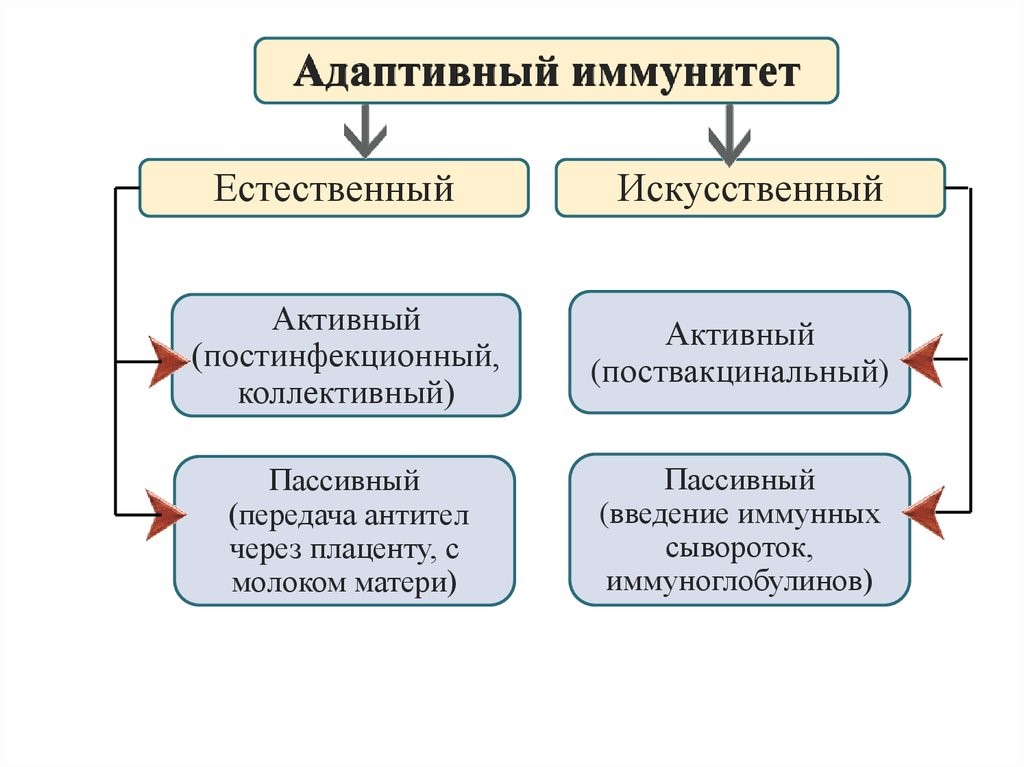
Приобретенный иммунитет (или адаптивный – от франц. adapter «приспосабливать») формируется индивидуально в течение жизни под влиянием антигенной стимуляции и, в свою очередь, подразделяется на естественный и искусственный (рис.16).
Естественный иммунитет формируется при встрече с патогеном, в результате чего в организме вырабатываются защитные иммунные факторы (активный естественный иммунитет), либо они попадают в готовом виде из материнского оргазма в период внутриутробного развития или при грудном вскармливании (пассивный естественный иммунитет).
Искусственный иммунитет создается путем введения вакцин или анатоксинов, которые стимулируют выработку антител против конкретных патогенов или их ядов. При этом с профилактической целью воспроизводится процесс реакции иммунной системы пациента на патоген, но в бессимптомной или легкой клинической форме с сохранением их защитной иммунной силы в течение нескольких месяцев, лет или даже пожизненно (искусственный активный иммунитет). Когда необходимо быстро и на короткое время защитить пациента от реального риска встречи с патогеном во время эпидемии или нейтрализовать уже проникший в его организм патоген применяются иммуноглобулины (антитела) как в очищенном виде, так и в дозированных объемах плазмы или сыворотки, полученных из крови донора (человека или животного). Применение готовых антител формирует пассивный искусственный иммунитет, сохраняющийся 2-3 недели.
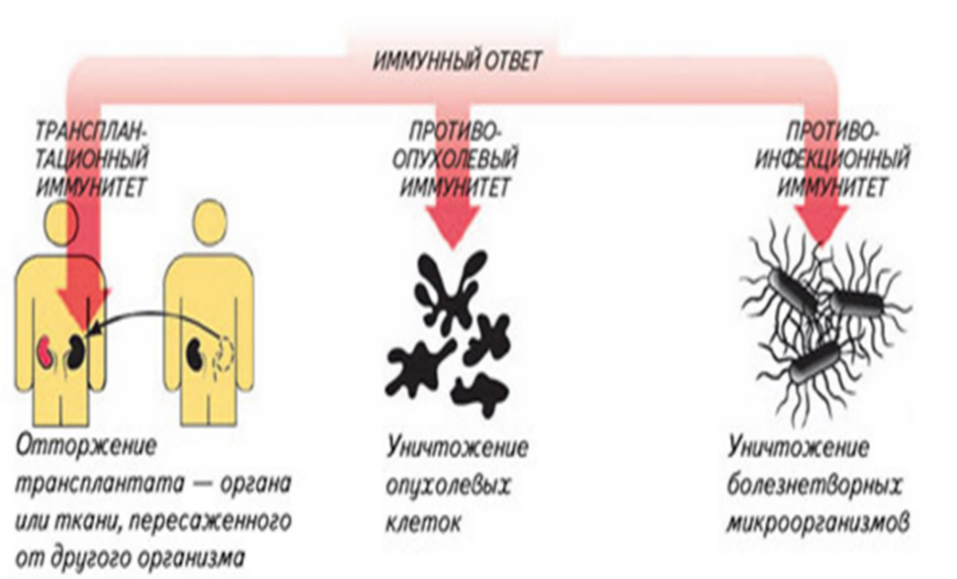
Адаптивный иммунитет основывается на трех главных процессах:
Рис.17.Варианты реагирования иммунной системы на пересадку органов или тканей, возникновение злокачественных новообразований и инфекций
Иммунокомпетентными клетками адаптивного иммунитета являются лимфоциты, которые живут в организме человека от нескольких месяцев до несколько лет. По функциям клетки подразделяются на Т-лимфоциты – 80% и В-лимфоциты – 20%.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием процесса, называемого селекцией, которая происходит в тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид.
Для активации Т-лимфоцита нужно, чтобы он получил специальные сигналы от рецепторов лейкоцитарной антигенной системы и коктейля из множества провоспалительных цитокинов.
С помощью специальных реагентов определяются маркеры поверхностных белков лейкоцитов определенного типа, которые называются кластерами дифференциации (Сluster of differentiation) – CD. В настоящее время известно 350 CD-антигенов и их подтипов (табл. 1).
Таблица 1. Главные идентификациионные СD-маркёры клеток
Лимфоидная стволовая клетка
CD19, CD72, CD79 и др.
Т-лимфоциты распознают клетки, несущие чужеродные антигены, и уничтожают их после непосредственного контакта (атаки), а также выполняют функцию регуляции иммунного ответа.
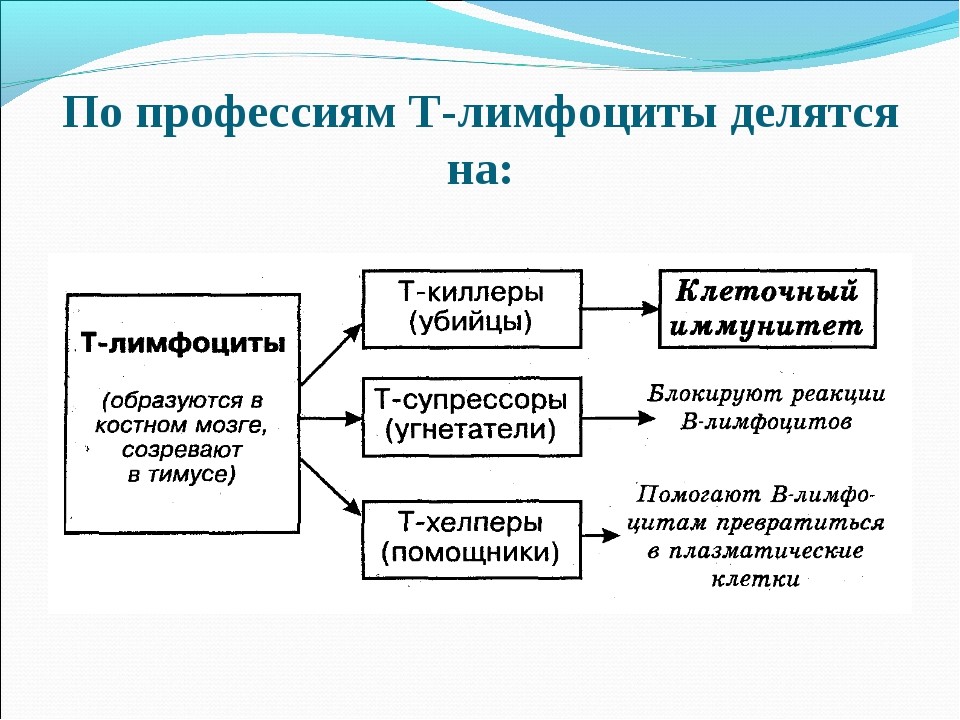
Т-лимфоциты имеют подтипы (рис. 18):
Рис. 18. Подтипы Т-лимфоцитов и их функции
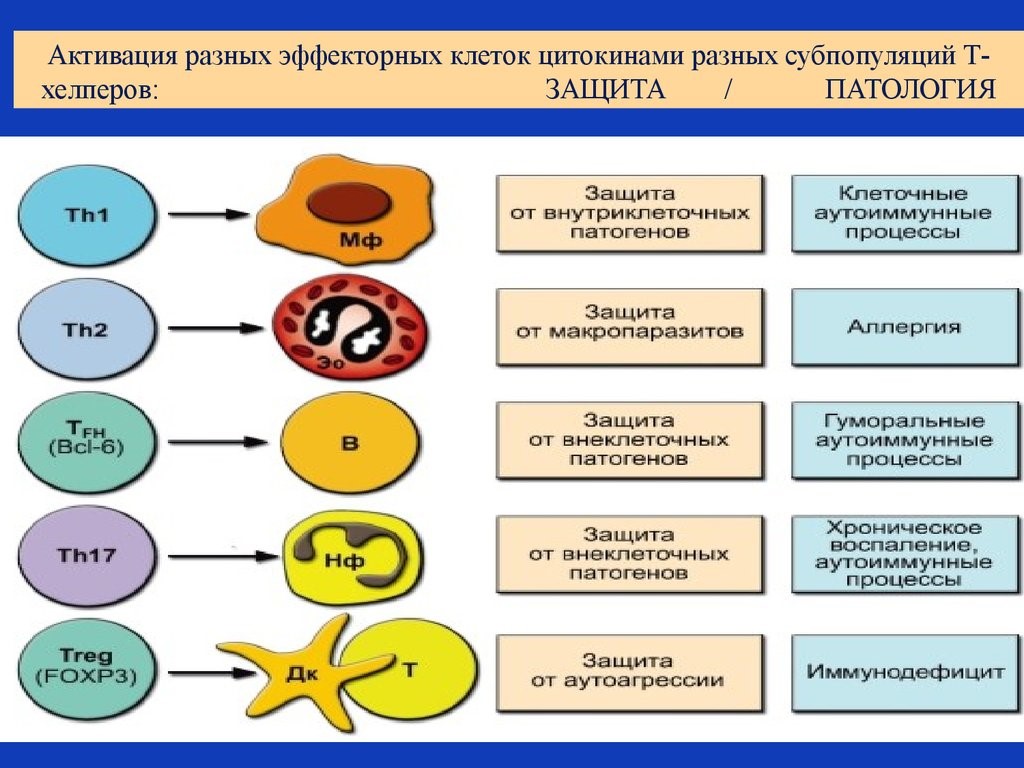
Рис. 19. Активация цитокинами разных субпопуляций Т-хелперов
Соотношение количества клеток CD4/CD8 называют иммунорегуляторным индексом (ИРИ). Если у пациента ИРИ повышен (более 2,2), то это говорит о чрезмерной активности T-хелперов и ослаблении регулирующей функции T-киллеров. При таком показателе иммунные клетки могут разрушать собственные ткани организма. Повышенный ИРИ чаще всего отмечается у пациентов с аутоиммунными болезнями (системной красной волчанкой, склеродермией, ревматоидным артритом и др.). Причиной чрезмерной активности T-хелперов может также стать опухоль вилочковой железы. При этой патологии продуцируется избыточное количество лимфоцитов. Высокие показатели ИРИ отмечаются при остром лимфобластном лейкозе. Это тяжелое онкологическое заболевание сопровождается неконтролируемым увеличением количества незрелых лимфоцитов.
Если иммунорегуляторный индекс понижен (менее1,6), то это говорит о серьезном ухудшении работы иммунитета. Низкие показатели ИРИ свидетельствуют о том, что в организме ослаблена функция защитных клеток, а регуляция со стороны T-киллеров чрезмерна. Обычно это отмечается при следующих патологиях, сопровождающихся иммунодефицитом: инфекционных болезнях (в том числе ВИЧ-инфекции); врожденном иммунодефиците; любых затяжных и хронических болезнях; опухолях костного мозга.
В-лимфоциты ответственны за гуморальное звено иммунитета – продукцию антител. После антигенного стимула В-лимфоцит превращается в лимфобласт – клетку, способную к делению. Часть лимфобластов дифференцируется в В-лимфоциты памяти, другая часть превращается в плазматические клетки, которые осуществляют продукцию антител.
В-лимфоциты несут на своей поверхности В-клеточный рецептор. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип – плазматические клетки, живущие до трех недель и обладающие уникальной способностью секретировать в этот срок тысячи антител.
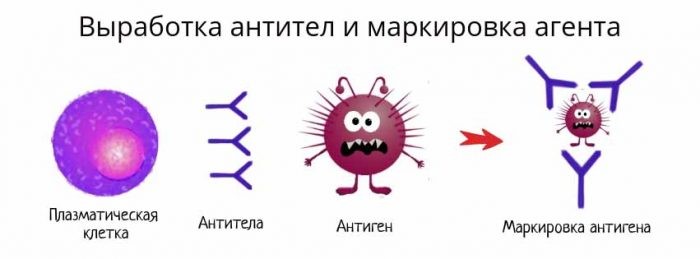
Антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Рис. 20. Выработка антител и маркировка патогена
Различают несколько классов антител (иммуноглобулинов). Первыми после антигенного раздражения, вызывающих агглютинацию бактерий и нейтрализацию вирусов, появляются иммуноглобулины М (IgM). В длительном иммунитете участвуют иммуноглобулины G(IgG).
В табл.2 представлена интерпретация лабораторных исследований на наличие патогена на молекулярном уровне и с помощью тестов на иммуноглобулины М и G.
Таблица 2. Интерпретация лабораторных исследований на наличие патогена на молекулярном уровне
Результат молекулярного исследования
Инфицированный или повторно инфицированный пациент
Ранние стадии инфекции. Требуется дополнительное исследование
Инфекция. Требуется дополнительное исследование
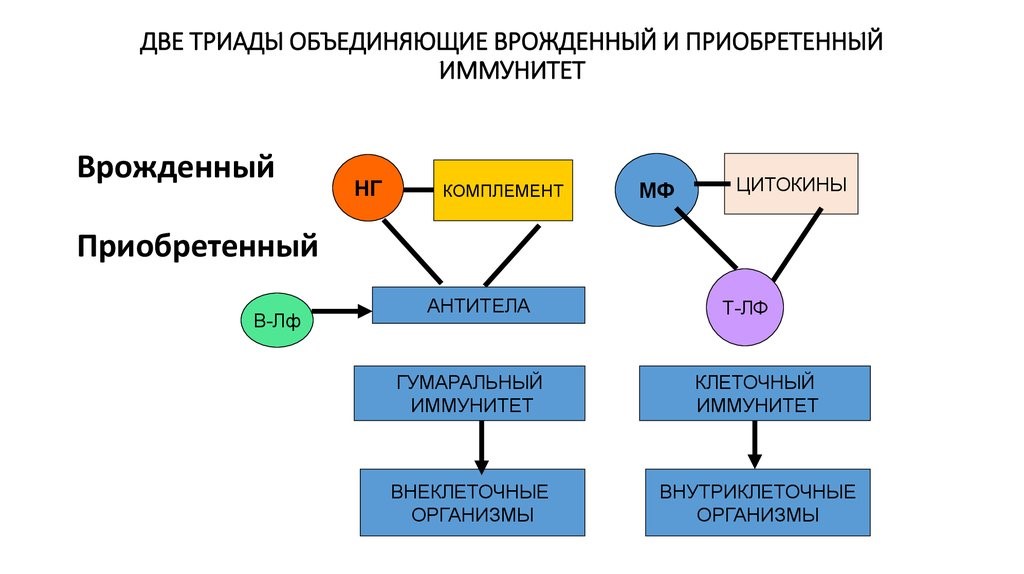
Врожденный и приобретенный виды иммунитета имеют точки соприкосновения, которые представляют две триады (рис.21)
Рис. 21. Две триады, объединяющие врожденный и приобретенный виды иммунитета
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и, если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ (рис.22).
Рис.22. Т-клетки памяти быстро формирует вторичный иммунный ответ
Иммунологическая толерантность
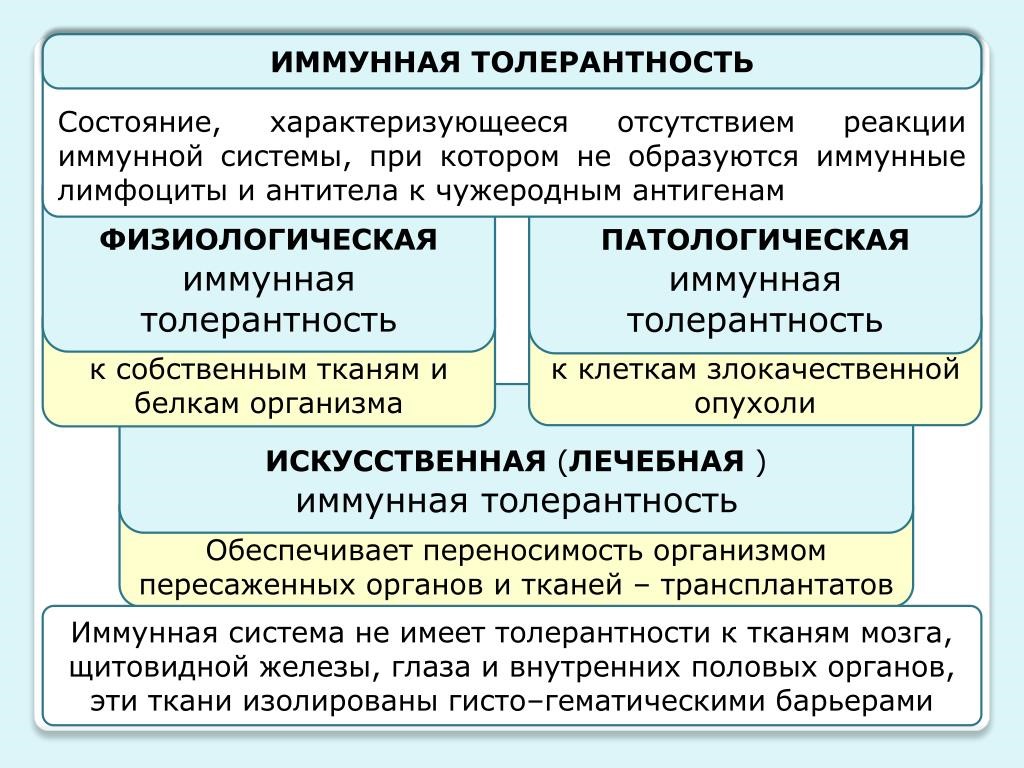
Под иммунологической толерантностью (терпимостью, ареактивностью) понимают отсутствие иммунного ответа на специфический антиген. Перечень антигенов, к которым может развиваться толерантность, практически неотличим от набора антигенов, против которых развивается специфический иммунный ответ (рис.23).
Рис. 23. Иммунная толерантность
Механизмы толерантности необходимы, поскольку иммунная система продуцирует огромное число разнообразных антиген специфичных рецепторов, и некоторые из них оказываются специфичными к собственным антигенам организма; толерантность предотвращает нежелательные реакции против собственных органов и тканей, также для нормального протекания беременности.
Нарушения иммунной системы у человека
Нарушения в работе иммунной системы можно подразделить на три категории: иммунодефициты, аутоиммунные заболевания и реакции гиперчувствительности.
Иммунодефициты
Иммунодефицит – снижение количественных показателей и/или функциональной активности основных компонентов иммунной системы, приводящее к нарушению защиты организма от патогенных микроорганизмов и проявляющееся повышенной инфекционной заболеваемостью.
Первичные иммунодефициты (ПИД) – наследственные заболевания, обусловленные дефектами генов, контролирующих иммунный ответ. В основном ПИД заявляют о себе уже в раннем детском возрасте, но иногда лишь к 30-40 годам жизни.
По механизмам развития выделяют 4 основные группы ПИД (табл.3):
Таблица 3. Некоторые первичные иммунодефициты
Частые бактериальные инфекции
Дефицит или полное отсутствие В-лимфоцитов
Антибиотики, пожизненное введение IgG
Частые респираторные инфекции, отиты
Дефекты Т- и В- лимфоцитов
Антибиотики, пожизненное введение IgG
Атаксия-телеангиоэкстазия (синдром Луи-Бар)
Аномалия двигательной функции, слабость мышц, нарушение речи
Дефицит Т- и В- лимфоцитов
ПИД, обусловленные дефектами фагоцитоза
Хроническая гранулёматозная болезнь
Частые пневмонии, гнойные инфекции
Пожизненная антибактериальная и противогрибковая терапия, интерферон гамма
ПИД, обусловленные дефектами в системе комплемента
Наследственный ангионевротический отек
Отеки губ и век при отсутствии зуда. Отеки гортани, носа, языка опасны для жизни
Низкая концентрация ингибитора эстеразы С1
Введение концентрата ингибитора эстеразы С1
Как следует из табл.3, основным и часто единственным методом лечения большинства пациентов с первичными В-клеточными иммунодефицитами являются иммуноглобулины. Это лекарственные средства, получаемые из плазмы крови человека. Они призваны заменить защитные антитела, отсутствующие в иммунной системе, с целью предотвращения или остановки развития тяжелых инфекционных заболеваний. Сегодня в арсенале врача имеются иммуноглобулины, различающиеся по концентрации активного вещества (5 и 10%), а также по способу введения (внутривенный и подкожный).
ПИД может проявиться в любом возрасте. В зависимости от этого у пациента возникают своеобразные проблемы, требующие определенных видов поддержки на протяжении всей жизни (табл. 4).
Таблица 4. Необходимость в видах поддержки пациента с ПИД в различных возрастных группах
В возрасте от 0 до 14 лет требуется уход со стороны родителей, направленный на профилактику инфекций и на период лечения. Могут потребоваться: обучение на дому; оказание психологической помощи; социальная поддержка в приобретении лекарственных средств.
В подростковом возрасте (14-18 лет) дополнительно могут возникнуть потребности в продолжении непрерывного обучения, профессиональной ориентации, налаживании взаимоотношений со сверстниками, организации досуга.
В возрасте от 18 до 65 лет у пациентов чаще возникают инфекционные осложнения, а с ними и расходы на приобретение лекарственных средств, не подлежащих восполнению, а также проблемы с трудоустройством.
В пожилом возрасте (старше 65 лет) возникают потребности в материальной, социальной и психологической поддержке пациента с ПИД.
Аутоиммунная патология
Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом. Заболеваниями такого типа страдает около 5% человечества. В организме пациента развиваются боевые действия, напоминающие гражданскую войну: в атаку идут «свои против своих». В этой борьбе победителей нет – одни страдания.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани.
В качестве аналога можно привести созданную турками в ХIV веке янычарскую пехоту, в которую набирали юношей-христиан 8-16 лет, воевших против своих сородичей.
Т-клеточная аутоиммуннная агрессия хорошо изучена при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
Такие же клетки-янычары, не помнящие своего родства, прослеживаются среди В-лимфоцитов:
Например, вследствие срыва иммунологической толерантности происходит активация В-лимфоцитов, продуцирующих антитела. Это приводит к выраженному повышению выработки тиреоидных гормонов (Т4 и Т3), а также к увеличению щитовидной железы в размерах (гипертрофии). Патология носит название болезнь Грейвса.
Еще одним примером может быть миастения гравис, которая характеризуется слабостью скелетной мускулатуры вследствие образования аутоантител против структур, отвечающих за холинергическую передачу и сокращение мышечного волокна;
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность – наличие определенного варианта какого-либо гена.
Гиперчувствительность
Под гиперчувствительностью понимают чрезмерный иммунный ответ на какой-либо антиген. Реакции гиперчувствительности подразделяют на несколько типов в зависимости от их длительности и механизмов, лежащих в их основе:
Эффективные методы воздействия на иммунитет:
Спекулятивные методы вокруг иммунитета:
Заключение
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным со сложнейшими взаимодействиями между ними.
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный (адаптивный) виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции, которые представляют собой микроорганизмы, злокачественные опухолевые клетки, пересаженные органы и ткани.
Адаптивный иммунитет основывается на трех главных процессах: распознавание антигенов, их удаление (элиминация) и формирование иммунологической памяти.
Поломки в структуре иммунной системы приводят к развитию иммунодефицитов, аутоиммунным заболеваниям или реакции гиперчувствительности.
Иммунодефицит на генетическом уровне (первичный) или приобретенный (вторичный) может проявиться в любом возрасте и привести к повышенной инфекционной заболеваемости. В последние годы появились средства заместительной терапии, которые продлевают жизнь этим пациентам. Для повышения качества их жизни требуется не только обеспечение дорогостоящим лечением, но и организация поддержки со стороны семьи, психологов и социальных институтов.
Аутоиммунные заболевания и гиперчувствительность – это неспособность организма противостоять разбушевавшейся иммунной системе, которая перепутала свое и чужое.
К сожалению, ни одно из заболеваний иммунной системы медицина еще не научилась излечивать, а только применять заместительную терапию.
Эффективными профилактическими методами воздействия на иммунную систему являются вакцинация и здоровый образ жизни. Купить иммунитет в аптеке пока никому не удалось.