какой индекс у азота
Таблица валентности.
В таблице валентности приведены значения валентности элементов периодической таблицы Менделеева. Что такое валентность?
Точками здесь обозначаются неподеленные пары электронов, однако в структурных формулах их отмечают не каждый раз.
В химии принято, что валентность химических элементов можно узнать по группе (колонке) в таблице Менделеева. В действительности не всегда валентность элемента соответствует номеру группы, но в большинстве случаев определенная валентность по такому методу даст правильный результат часто элементы, в зависимости от разных факторов, имеют не одну валентность. Чтобы проще было понимать и не путаться, ниже приведена таблица валентностей всех элементов периодической таблицы.
Цифра положительной валентности элемента соответствует количеству отданных атомом электронов, а отрицательной валентности – количеству электронов, которые атом должен забрать себе для завершения внешнего энергетического уровня.
Значение, приведенное в скобках таблицы валентности, перечисляет менее распространенные валентности. Если у элемента указана только одна цифра, значит он может иметь только одну валентность.
Таблица валентности химических элементов.
Порядковый номер химического элемента, он же: атомный номер, он же: зарядовое число атомного ядра, он же: атомное число
Русское / Английское наименование
Валентность и степень окисления
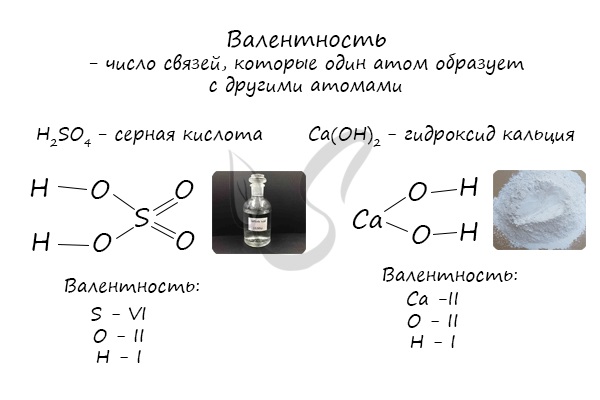
Валентность
Определяют валентность по числу связей, которые один атом образует с другими. Для примера рассмотрим две молекулы
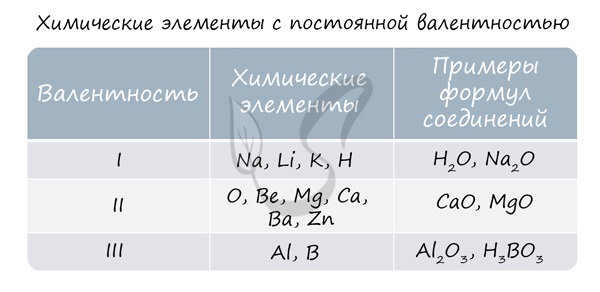
Для определения валентности нужно хорошо представлять графические формулы веществ. В этой статье вы увидите множество формул. Сообщаю вам также о химических элементах с постоянной валентностью, знать которые весьма полезно.
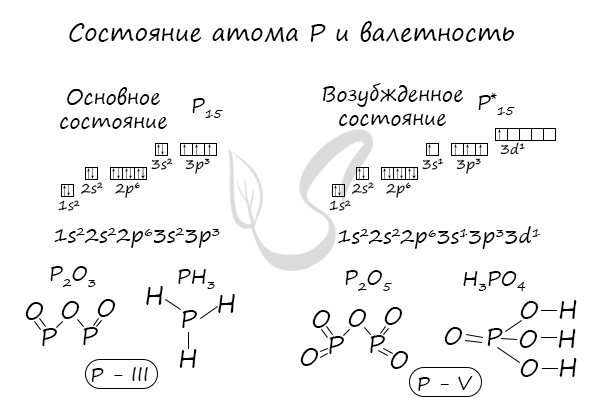
В электронной теории считается, что валентность связи определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии. Мы касались с вами темы валентных электронов и возбужденного состояния атома. На примере фосфора объединим эти две темы для полного понимания.
Подавляющее большинство химических элементов обладает непостоянным значением валентности. Переменная валентность характерна для меди, железа, фосфора, хрома, серы.
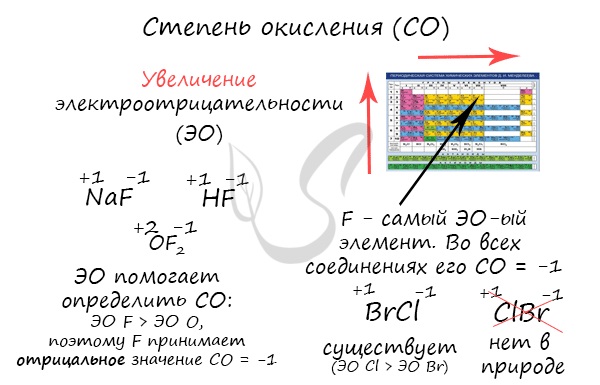
Степень окисления
Численно степень окисления равна условному заряду, который можно приписать атому, руководствуясь предположением, что все электроны, образующие связи, перешли к более электроотрицательному элементу.
Зная изменения электроотрицательности в периодах и группах периодической таблицы Д.И. Менделеева, можно сделать вывод о том какой элемент принимает «+», а какой минус. Помогают в этом вопросе и элементы с постоянной степенью окисления.
Самостоятельно определите степени окисления атомов в следующих веществах: RbOH, NaCl, BaO, NaClO3, SO2Cl2, KMnO4, Li2SO3, O2, NaH2PO4. Ниже вы найдете решение этой задачи.
Сравнивайте значение электроотрицательности по таблице Менделеева, и, конечно, пользуйтесь интуицией 🙂 Однако по мере изучения химии, точное знание степеней окисления должно заменить даже самую развитую интуицию 😉
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Валентность и степень окисления
Оксиды азота (NOx) Различные составы и номенклатуры
оксиды азота они представляют собой газообразные неорганические соединения, которые содержат связи между атомами азота и кислорода. Его группа химическая формула НЕТх, показывая, что оксиды имеют разные пропорции кислорода и азота.
Азот возглавляет группу 15 таблицы Менделеева, тогда как группа кислорода 16; оба элемента являются членами периода 2. Эта близость является причиной того, что связи N-O являются ковалентными в оксидах. Таким образом, связи в оксидах азота являются ковалентными.
Все эти связи могут быть объяснены с использованием теории молекулярной орбитали, которая раскрывает парамагнетизм (электрон, неспаренный на последней молекулярной орбитали) некоторых из этих соединений. Из них наиболее распространенными соединениями являются оксид азота и диоксид азота..
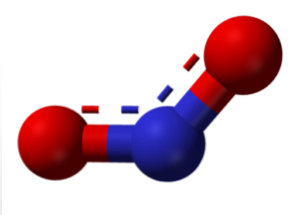
Молекула на верхнем изображении соответствует угловой структуре в газовой фазе диоксида азота (NO2). В отличие от оксида азота (NO) имеет линейную структуру (с учетом sp-гибридизации для обоих атомов).
Высокие температуры лучей разрушают энергетический барьер, который предотвращает протекание этой реакции в нормальных условиях. Какой энергетический барьер? Это образовано тройной связью N≡N, что делает N-молекулу2 инертный газ из атмосферы.
Числа окисления для азота и кислорода в их оксидах
Сколько электронов может разделить азот с кислородом? Если вы поделитесь электронами своей валентной оболочки один за другим, вы достигнете предела в пять электронов, что соответствует степени окисления +5.
Следовательно, в зависимости от того, сколько связей он образует с кислородом, степень окисления азота варьируется от +1 до +5..
Различные формулировки и номенклатуры
Оксиды азота в порядке возрастания степени окисления азота:
— N2Или закись азота (+1)
— НЕТ2, диоксид азота (+4)
Закись азота (N2O)
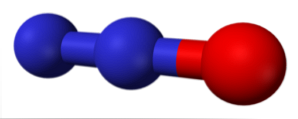
Закись азота (или широко известный как веселящий газ) представляет собой бесцветный газ со слабым сладким запахом и мало реактивным. Это может быть визуализировано как молекула N2 (синие сферы), который добавил атом кислорода на одном конце. Он готовится путем термического разложения нитратных солей и используется в качестве анестезирующего и обезболивающего средства..
Азот имеет степень окисления +1 в этом оксиде, что означает, что он не очень окислен и его потребность в электронах не является убедительной; однако вам нужно всего лишь получить два электрона (по одному на каждый азот), чтобы стать стабильным молекулярным азотом.
В основных и кислых растворах реакции:
Эти реакции, хотя и термодинамически благоприятны для образования стабильной молекулы N2, происходят медленно, и реагенты, которые дарят пару электронов, должны быть очень сильными восстановителями.
Оксид азота (NO)
Этот оксид состоит из бесцветного, реактивного и парамагнитного газа. Как и закись азота, он имеет линейную молекулярную структуру, но с большой разницей, что связь N = O также имеет характер тройной связи..
NO быстро окисляется в воздухе с образованием NO2, и, таким образом, генерировать более стабильные молекулярные орбитали с более окисленным атомом азота (+4).
Биохимические и физиологические исследования стоят за доброкачественной ролью этого оксида в живых организмах..
Он не может образовывать N-N-связи с другой молекулой NO из-за делокализации неспаренного электрона на молекулярной орбитали, который направлен больше на атом кислорода (из-за его высокой электроотрицательности). Противоположное происходит с NO2, которые могут образовывать газообразные димеры.
Триоксид азота (N2О3)
Почему это диссоциировано? Поскольку числа окисления +2 и +4 более стабильны, чем +3, последние присутствуют в оксиде для каждого из двух атомов азота. Это, опять же, может быть объяснено стабильностью молекулярных орбиталей в результате диспропорции.
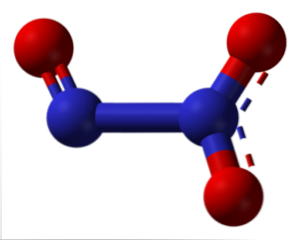
На изображении, левая сторона N2О3 соответствует NO, а правая сторона к NO2. Логично, что это происходит путем слияния предыдущих оксидов при очень низких температурах (-20ºC). N2О3 ангидрид азотной кислоты (HNO2).
Диоксид и тетроксид азота (NO2, N2О4)
НЕТ2 это коричневый или коричневый газ, реактивный и парамагнитный. Поскольку он имеет неспаренный электрон, он димеризуется (связывается) с другой газообразной молекулой NO2 с образованием четырехокиси азота, бесцветного газа, устанавливая баланс между двумя химическими веществами:
Точно так же НЕТ2 участвует в сложных атмосферных реакциях, вызывающих изменения концентрации озона (ИЛИ3) на земных уровнях и в стратосфере.
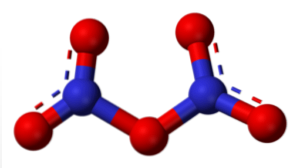
Пентоксид азота (N2О5)
Азотемия
Медицинский эксперт статьи
Одним из вариантов нефротоксических поражений является азотемия – это состояние, сопровождающееся нарушением почечной функции на фоне избыточного содержания в кровотоке азотных соединений. Если течение такой патологии тяжелое, то возможно быстрое развитие острой почечной недостаточности.
Если перевести название «азотемия» с латинского языка, то оно буквально означает «азот в кровотоке». Иногда это состояние называют уремией – то есть, «мочой в кровотоке», но эти понятия не совсем одинаковы: азотемия обычно является основой уремии.
Суть патологии заключается в том, что при распаде белка выделяются такие азотистые соединения, как мочевая кислота, мочевина, креатинин, аммиак, пурины и индикан. Присутствие таких продуктов в крови и обусловливает развитие азотемии.
Код по МКБ-10
Эпидемиология
Интересно, что многие аспекты азотемии до сих пор остаются неясными. С учетом сказанного, азотемия довольно распространена, на нее приходится от 8% до 16% госпитализаций и, более того, она связана со значительно более высоким риском смерти. [1]
Азотемия является единственным достоверным критерием развития почечной недостаточности, в том числе и хронической её формы, при которой показатели сывороточного креатинина превышают 0,18 ммоль/литр, а мочевины – 8 ммоль/литр (норма – 0,12 ммоль/литр и 6 ммоль/литр соответственно). Об уремии говорят при понижении массы функционирующих нефронов менее 20-25% от необходимого количества, и при выраженной азотемии (уровень креатинина больше 0,45 ммоль/литр, при мочевине больше 25-30 ммоль/литр).
Частота первичного обнаружения азотемии составляет 5-20 случаев на сотню населения в год. Чаще всего патологию диагностируют у пациентов 45-65 лет. [2]
Причины азотемии
Кровь непрерывно фильтруется почками, что необходимо для выведения продуктов жизнедеятельности и поддержания электролитного равновесия в системе кровообращения. При уменьшении притока крови к почкам фильтрация притормаживается, что приводит к скоплению продуктов, которые должны выводиться из организма. Такое состояние может достигать уровня интоксикации.
Скопление азотистых соединений (к примеру, мочевины и креатинина) типично для состояния азотемии и способно значительно осложнить работу организма. Подобная патология провоцируется любыми нарушениями, ухудшающими почечное кровообращение – в том числе, недостаточной сердечной деятельностью, шоковым состоянием, обезвоживанием, сильной кровопотерей и пр. [3]
В целом, речь идет о таких причинах азотемии:
Азотемия может сочетаться и проявляться на фоне других патологий.
Факторы риска
Опасными факторами, имеющими значение в развитии азотемии, могут стать:
В группу риска развития азотемии входят пациенты с повышенным уровнем артериального давления, сахарным диабетом, ожирением, а также лица в возрасте старше 50 лет, с различными заболеваниями почек (в том числе семейными), курильщики. Людям, входящим в группу риска, рекомендуется регулярно посещать врача для профилактического осмотра и сдачи основных клинических анализов. [4]
Патогенез
Мочевина является финальным продуктом белкового распада в организме, образуется в печени. В ходе выведения мочевины почками происходит выведение остатков «лишнего» азота. Частично выводится потовыми железами (что обусловливает специфический «аромат» пота).
Мочевина позволяет сохранять влагу в организме, нормализует минеральный обмен. Однако избыток этого вещества вредит тканям и органам. Его уровень зависит от равновесия процессов выработки и выведения из организма. Понижение концентрации отмечается на фоне низкобелкового питания, голодания, а также при печеночных патологиях, химических интоксикациях (мышьяком, фосфоросодержащими веществами), во время беременности или гемодиализа.
Клинически значимой считается азотемия, вызванная такими причинами:
Азотемия вызывает увеличение присутствия в кровотоке мочевины, креатинина, мочевой кислоты, метилгуанидина, фосфатов и пр. Мочевина и креатинин прямо зависимы от степени дисфункции нефронов. Информация о токсичном воздействии креатинина отсутствует, а вот избыточное количество мочевины способно приводить к головной боли, апатии, миастении, артритам. С развитием хронической почечной недостаточности нарушается тубулярно-гломерулярный баланс, повышается белковый катаболизм. [5]
Симптомы азотемии
Клиническая картина при азотемии развивается по нарастающей прогрессии, в зависимости от поражения определенных органов и систем, а также от повышения уровня азотистых соединений в системе кровообращения.
Базовыми симптомами считаются такие:
На начальной стадии пациенты жалуются на появление слабости, утомляемость, апатию, ухудшение аппетита. Рано отмечаются признаки анемии, обусловленные кровопотерей, недостатком железа и сиженным образованием эритропоэтина. Со временем общая слабость и сонливость нарастают, появляется апатия (уремическая энцефалопатия), ослабление мышц с судорожными подергиваниями, возникает зуд кожи, парестезии, кровоточивость. Возможно развитие псевдоподагры. Симптоматика может нарастать стремительно или постепенно.
Картина тяжелой, необратимой при диализе, азотемии включает в себя выраженные диспептические явления (неукротимую рвоту, диарею, анорексию), стоматогингивит, хейлит, побледнение и пожелтение лица, сухость кожи. Значительно повышается артериальное давление, отмечается кардиомегалия, регинопатия, застойная сердечная недостаточность. Поражается костная система в виде остеопороза, остеомаляции. Неврологические симптомы представлены миопатиейи энцефалопатией.
У пациентов пожилого возраста нарастают признаки коронарного атеросклероза.
Первые признаки
Адекватное количество азота в кровотоке приравнивается к 18-40 мг/литр. Если это содержание по каким-либо причинам повышается, то говорят о развитии патологии, а именно – об азотемии.
Врачи говорят о таких основных признаках присутствия азота в крови:
Указанные признаки, как правило, сочетаются друг с другом и говорят о развитии почечной недостаточности. Если лечебные меры не будут приняты своевременно, то картина усугубляется, а шансы на излечение снижаются.
Изменения в полости рта при азотемии
На приеме у врача при осмотре пациентов с азотемией можно отметить такие симптомы:
Пациенты жалуются на сухость в ротовой полости, боль в деснах, кровоточивость, изменение вкусовых ощущений, появление металлического привкуса и неприятного запаха. У отдельных пациентов отмечается боль в языке или внутренней стороне щек. Частота указанных патологических признаков непостоянна. К примеру, сухость в ротовой полости выявляется в 20-30% случаев, кровоточивость десен – практически в каждом втором случае, нарушение вкуса – в 25% случаев, а уремический запах изо рта можно наблюдать практически у 80% пациентов.
Достаточно распространенным сопутствующим заболеванием при азотемии становится уремический стоматит. Патология развивается при повышении мочевины в сыворотке больше чем на 150 мг/мл, но полная картина появления нарушения пока не выяснена. Патологические элементы чаще обнаруживаются на внутренней поверхности языка и слизистой ротовой полости. Стоматит плохо реагирует на лечение до нормализации уровня мочевины в крови, после чего излечивается самостоятельно на протяжении нескольких недель.
Стадии
Течение хронической азотемии подразделяется на курабельную и терминальную стадии. Курабельная стадия полностью обратима при своевременном назначении лечения и устранении причины патологии. Если же речь идет о тяжелом случае, когда период анурии продолжается в течение нескольких суток, то летальный исход может наступить в результате гиперкалиемии, ацидоза, нарушения водно-электролитного обмена.
Терминальная стадия характеризуется выраженным снижением клубочковой фильтрации с нарушением адаптивных механизмов почек. Ухудшают ситуацию повышенное артериальное давление, перикардит, нарушение кровообращения.
В терминальной стадии резко возрастает риск гибели пациента. Для продления жизни больного используют регулярный диализ. Летальный исход может наступить в результате нарушений сердечно-сосудистой деятельности, гиперкалиемии, инфекционных осложнений, сепсиса, геморрагий, а также вследствие развития уремической комы.
Формы
Азотемия имеет несколько классификаций, зависящих от причинного фактора появления нарушения. Однако все виды азотемии при почечной недостаточности обладают несколькими общими характеристиками: для них типично понижение скорости почечной клубочковой фильтрации и повышение азота мочевины в кровотоке и уровня креатинина в сыворотке. Используют индекс отношения азота мочевины к креатинину: этот показатель необходим для оценки типа азотемии. Нормальным индексным показателем считается
Контрагент ООО «АЗОТ-ИНДЕКС»
Краткое досье
| ИНН | 7725103373 |
| Находится | г. Москва, ул. Орджоникидзе aдрес |
| Возраст | 16 лет |
| Деятельность | нет данных |
| Масштаб деятельности | |
| Учредители | Артишева Евгения Юрьевна (0,5%; 5 тыс. руб.) |
| Руководитель | Артишева Евгения Юрьевна (генеральный директор) |
Обратите внимание
Полное досье контрагента
Общие сведения
Полное наименование организации: ООО «АЗОТ-ИНДЕКС»
ИНН: 7725103373
ОГРН: 1027700299142
Место нахождения: 115419, г. Москва, ул. Орджоникидзе, 11, 1/2
Статус организации: коммерческая, ликвидирована (прекращение деятельности юридического лица в связи с исключением из ЕГРЮЛ на основании п.2 ст.21.1 Федерального закона от 08.08.2001 №129-ФЗ)
Организационно-правовая форма: Общества с ограниченной ответственностью (код 12300 по ОКОПФ)
Регистрация в Российской Федерации
Организация ООО «АЗОТ-ИНДЕКС» зарегистрирована в едином государственном реестре юридических лиц 22 года назад 26 февраля 1999.
Чем занимается организация, виды деятельности
В ЕГРЮЛ отсутствует информация о видах деятельности организации.
Где находится ООО «АЗОТ-ИНДЕКС», юридический адрес
ООО «АЗОТ-ИНДЕКС» зарегистрировано по адресу: 115419, г. Москва, ул. Орджоникидзе, 11, 1/2. ( показать на карте )
По данному адресу также числятся следующие организации (включая ликвидированные):
Кто владелец (учредитель) организации
Учредителями ООО «АЗОТ-ИНДЕКС» являются:
| Учредители | доля | стоимость | с какой даты |
|---|---|---|---|
| ООО «АЗОТ-ИНДЕКС» (ликвидир. 09.11.2015) | 99,5% | 1 млн руб. | 26.02.1999 |
| Артишева Евгения Юрьевна (ИНН: 772608552203) | 0,5% | 5 тыс. руб. | 02.12.2010 |
Кто руководит ООО «АЗОТ-ИНДЕКС»
Руководителем организации (лицом, имеющем право без доверенности действовать от имени юридического лица) является генеральный директор Артишева Евгения Юрьевна (ИНН: 772608552203).
Кем руководит и владеет организация (числится учредителем)
В прошлом организация числилась учредителем в:
Финансы организации
Уставный капитал ООО «АЗОТ-ИНДЕКС» составляет 1 млн руб. Это значительно больше минимального уставного капитала, установленного законодательством для ООО (10 тыс. руб.).
Организация не применяет специальных режимов налогообложения (находится на общем режиме).
Лица, связанные с ООО «АЗОТ-ИНДЕКС»
На основе данных единого государственного реестра юридических лиц прослеживаются следующие взаимосвязи лиц, имеющих прямое или косвенное отношение к организации:
Последние изменения в ЕГРЮЛ
Представленные на этой странице данные получены из официальных источников: Единого государственного реестра юридических лиц (ЕГРЮЛ), Государственного информационного ресурса бухгалтерской отчетности (ГИР БО), с сайта Федеральной налоговой службы (ФНС), Минфина и Росстата. Указанные данные подлежат опубликованию в соответствии с законодательством РФ.
Разработкой программного обеспечения и обработкой информации занимается ООО «Профсофт» (ИНН 3906992381). Используется информация только из официальных открытых источников. Если вы заметили ошибку или некорректную информацию, пожалуйста, свяжитесь с разработчиком.