какой объем занимают 2400 моль кремния плотность кремния равна 2400 кг м3
Задача 1. Основываясь на характеристиках кристаллической структуры типа алмаза, рассчитайте следующие параметры кремния:



Основываясь на характеристиках кристаллической структуры типа алмаза, рассчитайте следующие параметры кремния:
а) число атомов, содержащихся в элементарной ячейке (единичном кубе);
б) атомный радиус структуры, полагая, что длина ребра элементарной ячейки кристалла кремния a ≈ 0,54 нм;
в) число атомов в 1 см 3 ;
г) число атомов, приходящихся на единицу площади в кристаллических плоскостях (111), (100) и (110). Приведенные значения индексов Миллера характеризуют положение плоскостей в кристалле. Три указанные здесь плоскости существенны для технологии полупроводниковых приборов;
д) удельную плотность, положив, что атомная масса кремния равна 28.
Решение:
а) Структура типа алмаза подобна кубической гранецентрированной структуре, каждой вершине которой принадлежит 1/8 атома, центру каждой грани – 1/2 атома. Однако здесь атом в центре тетраэдра чередуется с атомом, принадлежащим вершине (т.е. на каждую элементарную ячейку приходится дополнительно (1/2) 8 тетраэдров). Следовательно, число атомов в элементарной ячейке структуры типа алмаза составляет 8(1/8) + 6(1/2) + 4 = 8.
б) Атомный радиус представляет собой длину отрезка, соединяющего два ближайших узла. Решетку типа алмаза можно получить из двух кубических гранецентрированных решеток, если одну из них сместить по диагонали куба в соответствии с вектором трансляции (а/4, а/4, а/4). Тогда атомный радиус в решетке типа алмаза составит
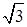
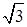
Число атомов в 1 см 3
 |
Рис. 7. Плоскости (111), (100) и (110)
Упражнение 11
Решение упражнений к учебнику Г.Я.Мякишева, Б.Б.Буховцева
1. Какую площадь может занять капля оливкового масла объемом 0,02 см3 при расплывании ее на поверхности воды?
2. Определите молярные массы водорода и гелия.
3. Во сколько раз число атомов в углероде массой 12 кг превышает число молекул в кислороде массой 16 кг?
4. Каково количество вещества (в молях), содержащегося в воде массой 1 г?
5. Молярная масса азота равна 0,028 кг/моль. Чему равна масса молекулы азота?
6. Определите число атомов в меди объемом 1 м3. Молярная масса меди М = 0,0635 кг/моль, ее плотность ρ = 9000 кг/м3.
7. Плотность алмаза 3500 кг/м3. Какой объем займут 1022 атомов этого вещества?
8. Под каким давлением находится газ в сосуде, если средний квадрат скорости его молекул v2 = 106 м2/с2, концентрация молекул n = 3 • 1025 м-3, масса каждой молекулы m0 = 5 • 10-26 кг?
9. В колбе объемом 1,2 л содержится 3 •1022 атомов гелия. Чему равна средняя кинетическая энергия каждого атома? Давление газа в колбе 105 Па.
10. Вычислите средний квадрат скорости движения молекул газа, если его масса m = 6 кг, объем V=4,9 м3 и давление р = 200 кПа.
Олимпиада по химии школьный этап 2021 ВОШ задания и ответы для 5-11 класса
ПОДЕЛИТЬСЯ
Задания и ответы школьного этапа 2021 олимпиады по химии для 5-11 класса всероссийской олимпиады школьников 2021-2022 учебного года, официальная дата проведения олимпиады в Омске: 12.10.2021 (12 октября 2021 года)
Интересные задания и ответы олимпиады:
1)Мы очень часто зимой любуемся на сказочные узоры, которые нарисовал мороз на стекле. Это кристаллическая вода. А какую кристаллическую решетку по форме имеют такие вещества: вода, алмаз, графит, поваренная соль, углекислый газ? Предложите рисунок кристаллической решетки каждого вещества.
2)Карбонат кальция известен также как кальцит, мел, мрамор, известняк. Его количественный состав представлен отношением: m(Са) : m(С) : m(О) = 10 : 3 : 12. Рассчитайте массовые доли каждого элемента в данном соединении.
3)Какую массу 20%-го раствора поваренной соли необходимо добавить к 50 г воды, чтобы
массовая доля соли стала 4%?
4)Составьте кроссворд из 45 клеточек, равному числу атомов в молекуле сахара С12Н22О11. В центре кроссворда слово «сахар». Всего слов не более 10 (со словом «сахар»). Все слова – это названия веществ, которые Вас окружают. Кроссворд не обязательно симметричной формы.
5)Дана смесь железных стружек, порошка мела, поваренной соли и порошка коллоидной серы. С помощью методов разделения смесей выделите отдельно каждое вещество.
6)Определите класс каждого соединения и составьте уравнения реакций, доказывающие принадлежность к данному классу: N2O, Tl2O3, BaO, SeO3, Cr2O3, Mn2O7, MnO, OF2, KO3.
7)Гидрокарбонат аммония нагрели. Полученную смесь газов пропустили над раскаленным углем. В результате получили два вещества, одно из которых вода. Второе вещество при сгорании образует газы, входящие в состав воздуха. Напишите уравнения четырех описанных реакций.
8)Сколько граммов осадка получится при охлаждении до 00С 300 мл раствора сульфата калия (плотность 1,2 г/мл), насыщенного при 300С. Растворимость сульфата калия при 300С равна 13 г. Растворимость сульфата калия при 00С равна 7,4 г.
9)Количественный состав вещества Х представлен отношением: m(K) : m(S) : m(О) = 39 : 32 : 64. Молярная масса вещества Х равна 270 г/моль. Найдите молекулярную формулу вещества Х и составьте его структурную формулу.
10)Вам предложены растворы веществ: серной кислоты, хлорида бария, карбоната натрия, хлорида железа (III). Получите максимально возможное количество других веществ, используя только предложенные исходные вещества и продукты их взаимодействия. Продемонстрируйте все полученные вещества. Составьте уравнения химических реакций, подтверждающие получение веществ.
11)Расположите вещества в порядке возрастания кислотных свойств: фенол, муравьиная кислота, стеариновая кислота, щавелевая кислота, глицерин, этиловый спирт. Объясните выбранный порядок, составьте уравнения реакций, подтверждающие кислотные химические свойства.
12)К раствору хлорида железа(III) добавили раствор сульфита натрия. Осадок отделили, высушили и прокалили. К твердому остатку добавили поташ и сплавили. Выделившийся газ прореагировал с аммиаком при 5000С. Напишите уравнения четырех описанных реакций.
13)Осуществить цепочку превращений: NaNa2O2NaOHNa[Al(OH)4] NaClNa Составить уравнения реакций, указать условия, при которых осуществимы эти реакции.
14)Сколько граммов осадка получится при охлаждении до 00С 300 мл раствора сульфата калия (плотность 1,2 г/мл), насыщенного при 300С. Растворимость сульфата калия при 300С равна 13 г. Растворимость сульфата калия при 00С равна 7,4 г.
15)Проведите ряд химических реакций получения хлорида хрома (III) из дихромата аммония, используя предложенные реактивы и оборудование. Получите и выделите хлорид хрома (III).
16)Малахит нагрели до 2000С. Полученный твердый остаток растворили в концентрированном растворе аммиака. В полученный раствор прилили уксусную кислоту, а затем раствор едкого натра. Напишите уравнения описанных реакций.
17)Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: при написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
18)При сжигании образца органического вещества А массой 6,36 г получено 8,96 л углекислого газа (н.у.) и 2,52 г воды. Данное вещество подвергается гидролизу в присутствии серной кислоты. Оба продукта гидролиза взаимодействуют с гидроксидом натрия. На нейтрализацию продуктов гидролиза, полученных из 1 моль вещества А, необходимо 4 моль гидроксида натрия. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества; 2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение гидролиза данного вещества в присутствии серной кислоты (используйте структурную формулу органического вещества).
19)Осуществите цепочку превращений неорганических веществ. Составьте уравнения реакций, подтверждающие превращения.
20)Вам предложена смесь порошков меди, алюминия и железа. С помощью реактивов разделите смесь и получите в отдельных пробирках сульфаты этих металлов.
Какой объем занимают 2400 моль кремния плотность кремния равна 2400 кг м3
10в-2 мм рт. ст.
Поверхностное натяжение расплавленного кремния, измеренное методом сидячей капли на подложках из ZrO2, TiO2 и MgO в атмосфере гелия при 1450° С, равно 730 дин/см.
Электрические свойства
Кремний по своим электрическим свойствам относится к типичным полупроводникам. С повышением температуры удельное электросопротивление кремния резко снижается. При плавлении он имеет электропроводность, свойственную жидким металлам.
При 300°К удельное электросопротивление кремния (р) зависит от содержания в нем примесей.
Кремний чистотой 98,5% имеет р = 0,8 ом*см, 99,97% —12,6 ом*см, спектрально-чистый кремний 30 ом*см. Наиболее чистые образцы кремния имеют р = 16 000 ом*см.
Ниже приведены некоторые теоретически рассчитанные электрические характеристики кремния, обладающего собственной проводимостью (при 300°С):
1713°С и температурой кипения 2590° С.
При охлаждении расплавленного кварца образуется прозрачное кварцевое стекло, которое служит одним из важнейших материалов для изготовления аппаратуры, применяемой в технологии производства кремния и других полупроводниковых материалов.
При нагревании SiO2 с углем при 2000—2200° С образуется карбид кремния SiC, обладающий полупроводниковыми свойствами.
Кремний образует довольно прочные соединения с галоидами, физико-химические свойства этих соединений приведены в табл. 57.













