при каком заболевании формируется гибус
СИНДРОМ ГИПЕРМОБИЛЬНОСТИ СУСТАВОВ в общей практике
Синдром гипермобильности суставов (ГМС) — нередкая причина обращения за медицинской помощью пациентов в любом возрасте. Клинические проявления СГМС многообразны и могут имитировать другие, более известные заболевания суставов. В связи с недостаточным
Синдром гипермобильности суставов (ГМС) — нередкая причина обращения за медицинской помощью пациентов в любом возрасте. Клинические проявления СГМС многообразны и могут имитировать другие, более известные заболевания суставов. В связи с недостаточным знакомством с данной патологией врачей-терапевтов, а в ряде случае ревматологов и ортопедов правильный диагноз часто не устанавливается. Традиционно внимание врача обращается на выявление ограничения объема движений в пораженном суставе, а не определение избыточного объема движений. Тем более что сам пациент никогда не сообщит о чрезмерной гибкости, так как он с детства с ней сосуществует и, более того, часто убежден, что и все люди имеют такие же возможности. Типичны две диагностические крайности: в одном случае, в связи с отсутствием объективных признаков патологии со стороны суставов (кроме просматриваемой гипермобильности) и нормальными лабораторными показателями у молодого пациента определяют «психогенный ревматизм», в другом — больному ставят диагноз ревматоидного артрита или заболевания из группы серонегативных спондилоартритов и назначают соответствующее, отнюдь не безобидное лечение.
Что считать гипермобильностью суставов?
Среди многих предложенных способов измерения объема движений в суставах общее признание получил метод Бейтона, представляющий собой девятибалльную шкалу, оценивающую способность обследуемого выполнить пять движений (четыре парных для конечностей и одно для туловища и тазобедренных суставов). Бейтон предложил упрощенную модификацию ранее известного метода Carter и Wilkinson (1964). Движения представлены на рис. 1.
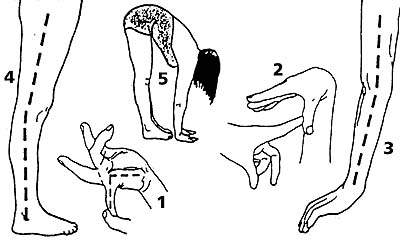 |
| Рисунок 1. Изменение объема движений 1. Пассивное разгибание мизинца кисти более 90°. 2. Пассивное прижатие большого пальца кисти к внутренней стороне предплечья. 3. Переразгибание в локтевом суставе более 10°. 4. Переразгибание в коленном суставе более 10°. 5. Передний наклон туловища с касанием ладонями пола при прямых ногах. |
Это простая и занимающая мало времени скрининговая процедура, получившая широкое распространение как в клинических, так и в эпидемиологических исследованиях. На основании ряда эпидемиологических работ были определены нормы подвижности суставов для здоровых людей. Степень подвижности суставов распределяется в популяции нормальным образом, то есть не по принципу «все или ничего», а в виде синусоидной кривой. Обычным для европейцев является счет по Бейтону от 0 до 4. Но средняя, «нормальная» степень подвижности суставов значительно отличается в возрастных, половых и этнических группах. В частности, при обследовании здоровых лиц в Москве в возрасте 16-20 лет среди женщин более половины, а среди мужчин более четверти демонстрировали степень ГМС, превышающую 4 балла по Бейтону. Таким образом, при отсутствии жалоб со стороны опорно-двигательного аппарата избыточная подвижность суставов в сравнении со средним показателем может рассматриваться как конституциональная особенность и даже возрастная норма. В связи с этим в педиатрической практике отсутствуют общепринятые нормы подвижности суставов — этот показатель значительно меняется в период роста ребенка.
Может ли избыточная гибкость суставов быть приобретена или это наследственная особенность?
Приобретенная избыточная подвижность суставов наблюдается у балетных танцоров, спортсменов и музыкантов. Длительные повторные упражнения приводят к растяжению связок и капсулы отдельных суставов. В этом случае имеет место локальная гипермобильность сустава (суставов). Хотя очевидно, что в процессе профессионального отбора (танцы, спорт) лица, изначально отличающиеся конституциональной гибкостью, имеют явное преимущество, фактор тренированности несомненно имеет место. Изменения в гибкости суставов наблюдаются также при ряде патологических и физиологических состояний (акромегалия, гиперпаратиреоидизм, беременность). Генерализованная ГМС является характерным признаком ряда наследственных заболеваний соединительной ткани, включающих синдром Марфана, несовершенный остеогенез, синдром Элерса–Данлоса. Это редкие заболевания. На практике врачу гораздо чаще приходится иметь дело с пациентами с изолированной ГМС, не связанной с тренировками и в ряде случаев сочетающейся с другими признаками слабости соединительно-тканных структур. Почти всегда удается установить семейный характер наблюдаемой ГМС и сопутствующей патологии, что свидетельствует о генетической природе наблюдаемого явления.
Определение синдрома гипермобильности суставов
Сам термин «синдром ГМС» принадлежит английским авторам Kirk, Ansell и Bywaters, которые в 1967 году обозначили таким образом состояние, при котором имелись определенные жалобы со стороны опорно-двигательного аппарата у гипермобильных лиц при отсутствии признаков какого-либо другого ревматического заболевания.
Последующие работы позволили конкретизировать нозологические границы данного синдрома, получившего определение «синдром доброкачественной гипермобильности суставов», в отличие от прогностически более тяжелых типов синдрома Элерса–Данлоса и других наследственных дисплазий соединительной ткани.
Последние, так называемые Брайтоновские критерии синдрома доброкачественной ГМС (1998) представлены в таблице. В данных критериях придается значение и внесуставным проявлениям слабости соединительно-тканных структур, что позволяет говорить о синдроме ГМС и у лиц с нормальным объемом движений в суставах (как правило, имеются в виду лица старшего возраста).
Распространенность синдрома гипермобильности суставов
Под синдромом ГМС понимают сочетание ГМС и каких-либо жалоб со стороны опорно-двигательного аппарата, обусловленных слабостью связочного аппарата. Истинная распространенность синдрома ГМС практически неизвестна. Конституциональная ГМС определяется у 7-20% взрослого населения. Хотя у большинства пациентов первые жалобы приходятся на подростковый период жизни, симптомы могут появиться в любом возрасте. Поэтому определения «симптоматичная» или «асимптоматичная» ГМС достаточно условны и отражают лишь состояние индивидуума с ГМС в определенный период жизни. Можно говорить о частоте выявления СГМС по данным отдельных клиник. Так, в одной из крупных европейских ревматологических клиник этот диагноз был установлен у 0,63% мужчин и 3,25% женщин из 9275 пациентов, поступивших на стационарное обследование. Но эти данные не отражают истинную картину, так как большинство пациентов с синдромом ГМС не нуждаются в стационарном лечении. По отечественным данным, доля пациентов с СГМС составляет 6,9% на амбулаторном приеме у ревматолога (Гауэрт В. Р., 1996). В связи с уже упоминавшимся недостаточным знанием врачей о данной патологии нередко эти пациенты регистрируются под другими диагнозами (ранний остеоартроз, периартикулярные поражения и т. д.).
Клинические проявления синдрома ГМС
Клиника СГМС многообразна и включает как суставные, так и внесуставные проявления, в общих чертах отраженные в упомянутых Брайтоновских критериях синдрома ГМС.
Существенную помощь в диагностике оказывает внимательный сбор анамнеза. Характерным фактом в истории жизни пациента является его особая чувствительность к физическим нагрузкам и склонность к частым травмам (растяжения, подвывихи суставов в прошлом), что позволяет думать о несостоятельности соединительной ткани. Выявляемый методом Бейтона избыточный объем движений в суставах дополняет собственно клинические формы проявления СГМС.
Суставные проявления
Внесуставные проявления. Данные признаки закономерны, так как основной структурный белок коллаген, первично участвующий в описываемой патологии, также присутствует в других опорных тканях (фасции, дерма, стенка сосудов).
Таким образом, при осмотре пациента с подозрением на СГМС, а это каждый больной молодого и среднего возраста с невоспалительным суставным синдромом, необходимо обращать внимание на возможные дополнительные признаки системной дисплазии соединительной ткани. Знание фенотипических проявлений синдрома Марфана и несовершенного остеогенеза позволяет исключить эти наследственные заболевания. В том случае если обнаруживаются явные кожные и сосудистые признаки (гиперэластичность кожи и спонтанное образование синяков без признаков коагулопатии), правомерно говорить о синдроме Элерса–Данлоса. Открытым остается вопрос дифференциальной диагностики синдрома доброкачественной ГМС и наиболее «мягкого», гипермобильного типа синдрома Элерса–Данлоса. С помощью Брайтоновских критериев это сделать невозможно, о чем авторы специально упоминают; в обоих случаях имеет место умеренное вовлечение кожи и сосудов. Ни для того, ни для другого синдрома не известен биохимический маркер. Вопрос остается открытым и будет, по-видимому, разрешен только с обнаружением специфического биохимического или генетического маркера для описываемых состояний.
Учитывая широкое распространение конституциональной ГМС в популяции, особенно среди молодежи, было бы ошибочным объяснять все суставные проблемы у данной категории лиц только гипермобильностью. Наличие ГМС отнюдь не исключает возможности развития у них любого другого ревматического заболевания, которым они подвержены с такой же вероятностью, как и лица с нормальным объемом движений в суставах.
Таким образом, диагноз синдрома ГМС становится обоснованным, когда исключены другие ревматические заболевания, а имеющиеся симптомы соответствуют клиническим признакам синдрома, логично дополняемым выявлением избыточной подвижности суставов и/или других маркеров генерализованного вовлечения соединительной ткани.
Лечение синдрома ГМС
Лечение пациента с синдромом ГМС зависит от конкретной ситуации. Разнообразие проявлений синдрома предполагает и дифференцированный подход к каждому отдельному пациенту. Важным моментом является объяснение в доступной форме причин его проблем с суставами («слабые связки») и убеждение пациента, что у него нет тяжелого заболевания, грозящего неизбежной инвалидностью. При умеренных артралгиях этого достаточно. Полезными будут рекомендации исключить нагрузки, вызывающие боли и дискомфорт в суставах. Решающими в лечении выраженных болей являются немедикаментозные методы, и в первую очередь — оптимизация образа жизни. Это предполагает приведение в соответствие нагрузок и порога их переносимости данным пациентом. Необходимо свести к минимуму возможности травм, что включает профессиональную ориентацию и исключение игровых видов спорта.
При упорных болях в одном или нескольких суставах используют эластичные ортезы (наколенники и т. п.). Очень важна своевременная коррекция выявляемого плоскостопия. При этом от врача требуются элементарные подологические знания — форма и жесткость стелек определяется индивидуально, от этого во многом зависит успешность лечения. Нередко удается справиться с упорными артралгиями коленных суставов единственно этим способом.
В обеспечении стабильности сустава существенную роль играют не только связки, но и окружающие сустав мышцы. Если путем упражнений повлиять на состояние связочного аппарата невозможно, то укрепление и повышение силы мышц — реальная задача. Гимнастика при синдроме ГМС имеет особенность — она включает так называемые «изометрические» упражнения, при которых происходит значительное напряжение мышц, но объем движений в суставах минимален. В зависимости от локализации болевого синдрома рекомендуют укреплять мышцы бедер (коленные суставы), плечевого пояса, спины и т. д. Полезно плавание.
Медикаментозная терапия применима как симптоматическое лечение при артралгиях. Так как боли при синдроме ГМС в основном имеют невоспалительную природу, то нередко можно видеть полное отсутствие эффекта от применения нестероидных противовоспалительных препаратов.
В этом случае большего результата можно добиться приемом анальгетиков (парацетамол, трамадол). Внутрисуставное введение кортикостероидов при отсутствии признаков синовита абсолютно неэффективно.
При периартикулярных поражениях (тендиниты, энтезопатии, бурситы, туннельные синдромы) тактика лечения практически не отличается от таковой у обычных пациентов. В умеренно выраженных случаях это мази с нестероидными противовоспалительными препаратами в виде аппликаций или компрессов; в более упорных — локальное введение малых доз глюкокортикостероидов, не обладающих местнодегенеративным действием (суспензия кристаллов метилпреднизолона, бетаметазона). Нужно отметить, что эффективность локальной терапии кортикостероидами в большой степени зависит от правильности постановки топического диагноза и техники выполнения самой процедуры.
Обратите внимание!
ГМС — распространенный ревматический синдром, не являющийся прогностически опасным, но вызывающий серьезные диагностические проблемы на практике. Пациент с предполагаемым синдромом ГМС требует от врача внимания к малозаметным деталям при сборе анамнеза и осмотре; необходимы знания и опыт в умении определить, насколько характер жалоб соответствует выявляемой необычной подвижности суставов. Лечение синдрома ГМС также имеет свою специфику и отличается от традиционной терапии других пациентов с заболеваниями суставов
Что сказать пациенту?
Важно объяснить пациенту в доступной форме причину его проблем с суставами («слабые связки») и убедить, что у него нет тяжелого заболевания, грозящего неизбежной инвалидностью. При умеренных артралгиях этого достаточно. Полезными будут рекомендации исключить нагрузки, вызывающие боли и дискомфорт в суставах; посоветовать свести к минимуму возможности травм, что включает соответствующую профессиональную ориентацию и исключение игровых видов спорта.
Врач объяснил, как расшифровать свои анализы на антитела к COVID-19
С результатами подобных анализов корреспондент «Российской газеты» обратилась к сертифицированному специалисту по физической реабилитации, члену Европейской ассоциации амбулаторной реабилитации Леониду Дьякову.
Антитела: иммунный ответ
Леонид Леонидович, в лаборатории люди получают результаты исследования, естественно, безо всяких комментариев. Их отправляют к врачам. Но к ним сейчас пробиться нелегко, да и не каждый рискует сидеть в очередях. В итоге человек мучительно вглядывается в непонятные обозначения, думает, плохо это или хорошо. Расскажите, что значит: «Антитела обнаружены».
Тест на антитела может показать, сталкивался ли человек с коронавирусом, даже если симптомов COVID-19 у него не было. Если антитела обнаружены, значит, организм среагировал на встреченный вирус. Они могут сохраняться, даже если самого вируса в организме уже нет. Этот тест говорит только о том, что произошел некий иммунный ответ.
Таким образом, выявление антител в крови является информативным свидетельством текущего или прошлого инфекционного процесса и помогает выявить стадию развития инфекции.
Обнаружение IgM указывает на недавнее инфицирование SARS-CoV-2. Они появляются непосредственно после контакта с носителем вируса, на третий-четвертый день. Через семь-десять дней они уже точно присутствуют в крови.
Потом они «стареют»?
Леонид Дьяков: Общий период вероятного выявления антител класса M не превышает двух месяцев. В течение этого времени IgM антитела постепенно полностью сменяются на IgG. Последние начинают формироваться в среднем на 21-й день.
Если еще есть IgM, и уже появились иммуноглобулины класса G, то это означает позднюю инфекцию. Просто IgM еще не сошли на нет.
Получается, наличие IgM не обязательно говорит об активной инфекции?
Леонид Дьяков: Да. Эти антитела могут выявляться и на стадии выздоровления.
Когда в крови выявляются только IgG, это говорит о том, что пациент выздоровел, и у него сформировался иммунитет к SARS-CoV-2. Если уровень IgG достаточно высок, то можно стать донором иммунокомпетентной плазмы. Например, IgG больше 40, а IgM больше 1,5, либо IgG больше 80, а IgM равно нулю.
То есть, если в крови выявлены обе группы антител, это означает, что человек уже выздоравливает?
Леонид Дьяков: Совершенно верно. Еще раз повторю: иммуноглобулины М говорят о том, что человек в данный момент болеет коронавирусом. Это не обязательно тяжелые формы, состояние может быть и бессимптомным. А иммуноглобулины G говорят о том, перенес ли он коронавирусную инфекцию в прошлом.
Далее, в графе «Дополнительная информация», вообще непонятная шифровка. А чем непонятнее, тем ведь страшнее. К примеру, вот передо мной результаты, переданные одним пациентом: «ОПсыв 0,0338; КП 1,45». Что кроется за этим?
От чего зависит количество антител в организме?
Лучше не болеть
Заразен ли человек, чей анализ мы расшифровываем?
Леонид Дьяков: По данному тесту нельзя определить, заразен ли еще человек. В принципе, с такими показателями, которые вы предоставили, пациент не заразен.
Но чтобы достоверно знать это, следует все же сдать еще мазок. Именно он покажет, выделяется ли вирус во внешнюю среду. Если он будет отрицательный, то человек стопроцентно не заразен. Без этой уверенности я бы рекомендовал соблюдение мер социальной дистанции и индивидуальной защиты даже в случае обнаружения только антител класса IgG.
А вы верите в то, что все должны переболеть, и тогда с эпидемией будет покончено?
Леонид Дьяков: В этом, конечно, есть логика. Но проблема в том, что вирус дает достаточно серьезные осложнения. И не все болеют в легкой или бессимптомной форме.
Люди, узнавшие что у них обнаружены антитела, начинают думать, когда же, где подхватили заразу. Вспоминают, когда болели. Может ли данный тест показывать антитела не только на COVID-19, но и на перенесенные другие ОРЗ или ОРВИ?
Леонид Дьяков: Исключено. Это специфичный тест именно на антитела к коронавирусной инфекции.
Человек припомнил, что сильно болел в феврале, ему было очень плохо. Мог тогда быть коронавирус?
Леонид Дьяков: Иммуноглобулин G с тех пор не сохранился бы.
То есть, носители антител могут, в принципе, радоваться, что переболели коронавирусом, практически не заметив этого?
Леонид Дьяков: Те, кто переболел легко или бессимптомно, вырабатывают низкий уровень иммуноглобулина G и могут заболеть повторно.
Чем тяжелее протекает заболевание, тем больше антител произведет иммунная система, и тем дольше они проживут в крови после болезни.
Однако есть информация, что сохраняются так называемые клетки памяти. Организм запоминает, как вырабатывать эти антитела, при каких условиях и в каком количестве. И в случае повторного контакта с вирусом организм начинает синтезировать IgG-антитела значительно быстрее, не за 21 день, а за три. И они способны «смягчать» течение заболевания, препятствовать развитию тяжелых осложнений.
Дышите глубже
Получается, что в принципе сдавать тест на антитела и не совсем нужно. Какая разница, болел человек или нет, если этого особо и не заметил, а никаких таких преимуществ наличие антител не дает. Все так же нужно предохраняться от заражения…
Леонид Дьяков: Мое личное мнение, если человек чувствует себя хорошо, особой надобности в тестировании нет. Ведь с тем же успехом можно поискать у себя вирус герпеса и другие.
Однако тестирование поможет решить проблему в более глобальном масштабе, выработать стратегию борьбы с коронавирусом, поскольку по количеству иммунных людей можно спрогнозировать, когда случится спад эпидемии.
Что делать тем, у кого обнаружены антитела класса IgM?
Леонид Дьяков: Если нет явных признаков заболевания, нужно побольше двигаться, гулять на свежем воздухе, дышать полной грудью, чтобы работали легкие, а кислород циркулировал в крови.
Все материалы сюжета «COVID-19. Мы справимся!» читайте здесь.
Невропатия седалищного нерва. Синдром грушевидной мышцы
Болезни периферической нервной системы — одна из наиболее частых причин инвалидизации пациентов трудоспособного возраста. В структуре этих болезней преобладающее место занимают болевые синдромы (Н. Н. Яхно, 2003; Г. Р. Табеева, 2004).
Болезни периферической нервной системы — одна из наиболее частых причин инвалидизации пациентов трудоспособного возраста. В структуре этих болезней преобладающее место занимают болевые синдромы (Н. Н. Яхно, 2003; Г. Р. Табеева, 2004). Причины развития невропатического болевого синдрома могут быть различными: сахарный диабет, паранеопластические процессы, ВИЧ, герпес, хронический алкоголизм (А. М. Вейн, 1997; И. А. Строков, А. Н. Баринов, 2002).
При поражении периферической нервной системы выделяют два типа боли: дизестезическую и трункальную. Поверхностная дизестезическая боль обычно наблюдается у пациентов с преимущественным поражением малых нервных волокон. Трункальная боль встречается при компрессии спинно-мозговых корешков и туннельных невропатиях.
У пациентов с этим видом болевого синдрома невозможно выбрать оптимальную стратегию лечения без идентификации патофизиологических механизмов. Поэтому при определении тактики терапии необходимо учитывать локализацию, характер и выраженность клинических проявлений болевого синдрома.
Под компрессионно-ишемической (туннельной) невропатией понимают невоспалительные поражения периферического нерва, развивающиеся под влиянием компрессии или ишемических воздействий.
В зоне компрессии соответствующего нерва нередко находят болезненные уплотнения или утолщения тканей, приводящие к существенному сужению костно-связочно-мышечных влагалищ, через которые проходят нервно-сосудистые стволы.
В настоящее время известно множество вариантов компрессионных невропатий. Их клиническая картина складывается из трех синдромов: вертебрального (в случаях участия одноименного фактора), неврального периферического, рефлекторно-миотонического или дистрофического. Вертебральный синдром на любом этапе обострения, и даже в стадии ремиссии, может вызывать изменения в стенках «туннеля». Миодистрофический очаг, выступающий в качестве реализующего звена, обусловливает невропатию на фоне своего клинического пика. Неврологическая картина компрессионных невропатий складывается из симптомов поражения той или иной выраженности в соответствующих мио- и дерматомах. Диагноз компрессионных невропатий ставится при наличии болей и парестезий в зоне иннервации данного нерва, двигательных и чувствительных расстройств, а также болезненности в зоне рецепторов соответствующего канала и вибрационного симптома Тинеля. При затруднениях в диагностике используются электронейромиографические исследования: определяются поражения периферического нейрона, соответствующего данному нерву, и степень уменьшения скорости проведения импульса по нерву дистальнее места его компрессии. Синдром грушевидной мышцы — самая распространенная туннельная невропатия. Патологическое напряжение грушевидной мышцы при компрессии корешка L5 или S1, а также при неудачных инъекциях лекарственных веществ ведет к сдавливанию седалищного нерва (или его ветвей при высоком отхождении) и сопровождающих его сосудов в подгрушевидном пространстве.
Для выбора правильной стратегии терапии необходимо четко знать основные клинические симптомы поражения той или иной области. Основные клинические проявления поражения нервов крестцового сплетения:
Наиболее трудны в плане диагностики поражения в области таза или выше ягодичной складки — из-за наличия соматической или гинекологической патологии у пациентов. Клинические симптомы поражения в области таза или выше ягодичной складки складываются из следующих вариантов нарушений двигательных и чувствительных функций.
Поражение седалищного нерва на уровне подгрушевидного отверстия может наблюдаться в двух вариантах:
Для компрессии седалищного нерва и идущих рядом сосудов характерны следующие клинические проявления: ощущение постоянной тяжести в ноге, боли тупого, «мозжащего» характера. При кашле и чихании усиления болей не наблюдается. Отсутствует атрофия ягодичной мускулатуры. Зона гипестезии не распространяется выше коленного сустава.
Синдром грушевидной мышцы встречается не менее чем у 50% больных дискогенным пояснично-крестцовым радикулитом. Если пациенту поставлен данный диагноз, предположение о наличии синдрома грушевидной мышцы может возникнуть при наличии упорных болей по ходу седалищного нерва, не уменьшающихся при медикаментозном лечении. Гораздо труднее определить наличие данного синдрома, если имеются только болевые ощущения в области ягодицы, носящие ограниченный характер и связанные с определенными положениями (перемещениями) таза или при ходьбе. Часто синдром грушевидной мышцы регистрируется в гинекологической практике. При синдроме грушевидной мышцы возможно:
Клиническая картина синдрома грушевидной мышцы состоит из локальных симптомов и симптомов сдавления седалищного нерва. К локальным относится ноющая, тянущая, «мозжащая» боль в ягодице, крестцово-подвздошном и тазобедренном суставах, которая усиливается при ходьбе, в положение стоя, при приведении бедра, а также в полуприседе на корточках; несколько стихает в положении лежа и сидя с разведенными ногами. При хорошем расслаблении большой ягодичной мышцы под ней прощупывается плотная и болезненная при натяжении (симптом Бонне–Бобровниковой) грушевидная мышца. При перкуссии в точке грушевидной мышцы появляется боль на задней поверхности ноги (симптом Виленкина). Клиническая картина сдавления сосудов и седалищного нерва в подгрушевидном пространстве складывается из топографо-анатомических «взаимоотношений» его больше- и малоберцовых ветвей с окружающими структурами. Боли при компрессии седалищного нерва носят тупой, «мозжащий» характер с выраженной вегетативной окраской (ощущения зябкости, жжения, одеревенения), с иррадиацией по всей ноге или преимущественно по зоне иннервации больше- и малоберцовых нервов. Провоцирующими факторами являются тепло, перемена погоды, стрессовые ситуации. Иногда снижаются ахиллов рефлекс, поверхностная чувствительность. При преимущественном вовлечении волокон, из которых формируется большеберцовый нерв, боль локализуется в задней группе мышц голени. В них появляются боли при ходьбе, при пробе Ласега. Пальпаторно отмечается болезненность в камбаловидной и икроножной мышцах. У некоторых больных сдавление нижней ягодичной артерии и сосудов самого седалищного нерва сопровождается резким переходящим спазмом сосудов ноги, приводящим к перемежающейся хромоте. Пациент вынужден при ходьбе останавливаться, садиться или ложиться. Кожа ноги при этом бледнеет. После отдыха больной может продолжать ходьбу, но вскоре у него повторяется тот же приступ. Таким образом, кроме перемежающейся хромоты при облитерирующем эндартериите существует также подгрушевидная перемежающаяся хромота. Важным диагностическим тестом является инфильтрация грушевидной мышцы новокаином с оценкой возникающих при этом положительных сдвигов. Рефлекторное напряжение в мышце и нейротрофические процессы в ней вызваны, как правило, раздражением не пятого поясничного, а первого крестцового корешка. Распознать указанный синдром помогают определенные мануальные тесты.
Поскольку болезненное натяжение грушевидной мышцы чаще всего связано с ирритацией первого крестцового корешка, целесообразно поочередно проводить новокаиновую блокаду этого корешка и новокаинизацию грушевидной мышцы. Значительное уменьшение или исчезновение болей по ходу седалищного нерва может рассматриваться как динамический тест, показывающий, что боли обусловлены компрессионным воздействием спазмированной мышцы.
Поражения седалищного нерва
Поражения седалищного нерва ниже выхода из малого таза (на уровне бедра и ниже) или в полости малого таза характеризуют следующие признаки.
Кроме вышеописанных клинических симптомов, вероятно развитие вазомоторных и трофических расстройств: повышение кожной температуры на пораженной ноге. Голень и стопа становятся холодными и цианотичными. Часто на подошве обнаруживаются гипергидроз или ангидроз, гипотрихоз, гиперкератоз. Появляются изменения цвета и формы ногтей, трофические нарушения на пятке, тыльной поверхности пальцев, наружном крае стопы, регистрируется снижение силы, а также атрофия мышц стопы и голени. Больной не может встать на носки или на пятки. Для определения начального поражения седалищного нерва можно использовать тест на определение силы полусухожильной, полуперепончатой и двуглавой мышц бедра.
Синдром седалищного нерва (ишемически-компрессионная невропатия седалищного нерва). В зависимости от уровня (высоты) поражения возможны разные варианты синдрома седалищного нерва.
Очень высокий уровень поражения (в тазу или выше ягодичной складки) характеризуется: параличом стопы и пальцев, утратой ахиллова и подошвенного рефлексов; анестезией (гипестезией) почти всей голени и стопы, кроме зоны n. sapheni; выпадением функций двуглавой мышцы бедра, полусухожильной, полуперепончатой мышц; гипестезией (анестезией) по задненаружной поверхности бедра; невозможностью вращения бедра кнаружи; наличием положительных симптомов натяжения (Ласега, Бонне); наличием вазомоторных и трофических расстройств (гипер- или гипотрихоз, гипо- или гипергидроз, изменение роста ногтей, образование трофических язв в области пятки и наружного края стопы).
Поражение на уровне подгрушевидного отверстия складывается из двух групп симптомов — поражения самой грушевидной мышцы и седалищного нерва. К первой группе симптомов относят: болезненность при пальпации верхневнутренней части большого вертела бедра (места прикрепления грушевидной мышцы к капсуле этого сочленения); болезненность при пальпации в нижней части крестцово-подвздошного сочленения; симптом Бонне (пассивное приведение бедра с ротацией его внутрь, вызывающее боли в ягодичной области, реже — в зоне иннервации седалищного нерва); болезненность при пальпации ягодицы в точке выхода седалищного нерва из-под грушевидной мышцы. Ко второй группе относятся симптомы сдавления седалищного нерва и сосудов. Болезненные ощущения при компрессии седалищного нерва характеризуются чувством постоянной тяжести в ноге, тупым, «мозжащим» характером боли, отсутствием усиления болей при кашле и чихании, а также атрофии ягодичной мускулатуры, зона гипестезии не поднимается выше коленного сустава.
Поражение на уровне бедра (ниже выхода из малого таза) и до уровня деления на мало- и большеберцовый нервы характеризуется: нарушением сгибания ноги в коленном суставе; специфической походкой; отсутствием активных движений в стопе и пальцах, которые умеренно отвисают; присоединяющейся через 2–3 нед атрофией парализованных мышц, часто маскирующей пастозность ноги; гипестезией (анестезией) по задненаружной поверхности голени, тылу стопы, подошве и пальцам; нарушением суставно-мышечной чувствительности в голеностопном суставе и в межфаланговых суставах пальцев стопы; отсутствием вибрационной чувствительности на наружной лодыжке; болезненностью по ходу седалищного нерва — в точках Валле и Гара; положительным симптомом Ласега; исчезновением ахиллова и подошвенного рефлексов.
Синдром неполного повреждения седалищного нерва характеризуется наличием болей каузалгического характера («жгучие» боли, усиливаются при опускании ноги, провоцируются легким прикосновением); резкими вазомоторными и трофическими расстройствами (первые 2–3 нед кожная температура на больной ноге на 3–5 °С выше («горячая кожа»), чем на здоровой, в дальнейшем голень и стопа становятся холодными и цианотичными). Часто на подошвенной поверхности обнаруживаются гипергидроз или ангидроз, гипотрихоз, гиперкератоз, изменения формы, цвета и темпа роста ногтей. Иногда возникают трофические язвы на пятке, наружном крае стопы, тыльной поверхности пальцев. На рентгенограммах выявляются остеопороз и декальцификация костей стопы.
Синдром начального поражения седалищного нерва может быть диагностирован путем использования тестов для определения силы полусухожильной и полуперепончатых мышц.
Синдром грушевидного, внутреннего запирательного нервов и нерва квадратной мышцы бедра. Полный синдром грушевидного, внутреннего запирательного нервов и нерва квадратной мышцы бедра характеризуется нарушением ротации бедра кнаружи. Синдром частичного поражения указанной группы нервов может диагностироваться на основании использования тестов для определения объема движений и силы обследуемого.
Синдром верхнего ягодичного нерва. Полный синдром верхнего ягодичного нерва характеризуется нарушением отведения бедра с частичным нарушением ротации последнего, затруднением поддержания вертикального положения туловища. При двустороннем параличе указанных мышц больному трудно стоять (стоит неустойчиво) и ходить (появляется так называемая «утиная походка» с переваливанием с бока на бок). Синдром частичного поражения верхнего ягодичного нерва можно выявить с помощью теста, определяющего силу ягодичных мышц. По степени снижения силы по сравнению со здоровой стороной делается заключение о частичном поражении верхнего ягодичного нерва.
Синдром нижнего ягодичного нерва. Полный синдром нижнего ягодичного нерва характеризуется затруднением разгибания ноги в тазобедренном суставе, а в положении стоя — затруднением выпрямления наклоненного таза (таз наклонен вперед, при этом в поясничном отделе позвоночника наблюдается компенсаторный лордоз). Затруднены вставание из положения сидя, подъем по лестнице, бег, прыжки. При длительном поражении указанного нерва отмечаются гипотония и гипотрофия ягодичных мышц. Синдром частичного поражения нижнего ягодичного нерва может диагностироваться с помощью теста для определения силы большой ягодичной мышцы. По степени снижения объема и силы указанного движения (и в сравнении их со здоровой стороной) делают заключение о степени нарушения функций нижнего ягодичного нерва.
Лечение
Терапия невропатии седалищного нерва требует знания этиологических и патогенетических механизмов развития заболевания. Тактика лечения зависит от тяжести и скорости прогрессирования заболевания. Патогенетическая терапия должна быть направлена на устранение патологического процесса и его отдаленных последствий. В остальных случаях лечение должно быть симптоматическим. Его цель — продление стойкой ремиссии и повышение качества жизни пациентов. Основным критерием оптимального лечебного воздействия на пациента является сочетание медикаментозных и немедикаментозных методов. Среди последних лидируют физиотерапевтические методики и методы постизометрической релаксации.
При нарушении функции мышц тазового пояса и нижней конечности рекомендуется использовать одну из техник мануальной терапии — постизометрическое расслабление (ПИР), т. е. растяжение спазмированной мышцы до ее физиологической длины после максимального напряжения. Основными принципами медикаментозной терапии поражений периферической нервной системы являются раннее начало лечения, снятие болевого синдрома, сочетание патогенетической и симптоматической терапии. Патогенетическая терапия направлена в первую очередь на борьбу с оксидантным стрессом, воздействием на микроциркуляторное русло, улучшение кровоснабжения пораженного участка, снятие признаков нейрогенного воспаления. С этой целью применяются антиоксидантные, вазоактивные и нестероидные противовоспалительные препараты (НПВП). Сложность медикаментозной терапии связана в большинстве случаев с запутанной анатомо-физиологической иерархией структур, вовлеченных в патологический процесс. Отчасти это обусловлено строением и функционированием структур пояснично-крестцового сплетения. В то же время базисным механизмом, лежащим в основе развития невропатии, является четкая корреляция между компрессией и ишемией нерва и развитием оксидантного стресса.
Оксидантный стресс — нарушение равновесия между продукцией свободных радикалов и активностью антиоксидантных систем. Развившийся дисбаланс приводит к усиленной продукции соединений (нейротрансмиттеров), выделяющихся поврежденными тканями: гистамин, серотонин, АТФ, лейкотриены, интерлейкины, простагландины, окись азота и т. д. Они приводят к развитию нейрогенного воспаления, увеличивая проницаемость сосудистой стенки, а также способствуют высвобождению тучными клетками и лейкоцитами простагландина E2, цитокинов и биогенных аминов, повышая возбудимость ноцицепторов.
В настоящее время появились клинические работы, посвященные использованию препаратов, улучшающих реологические свойства крови и эндотелийзависимые реакции стенки сосудов у пациентов с компрессионными невропатиями. Такие препараты, как производные тиоктовой кислоты (тиогамма, тиоктацид) и гинкго билоба (танакан), успешно применяются с целью уменьшения проявлений оксидантного стресса. Однако патогенетически более обосновано применение лекарственных средств, обладающих поливалентным механизмом действия (церебролизин, актовегин).
Приоритетность использования актовегина обусловлена возможностью его назначения для проведения лечебных блокад, хорошей сочетаемостью с другими лекарственными средствами. При компрессионно-ишемических невропатиях, как в острой, так и в подострой стадиях заболевания, целесообразно применение актовегина, особенно при отсутствии эффекта от других способов лечения. Назначается капельное введение 200 мг препарата в течение 5 дней, с последующим переходом на пероральное применение.
В механизмах развития заболеваний периферической нервной системы важное место занимают нарушения гемодинамики в структурах периферической нервной системы, ишемия, расстройство микроциркуляции, нарушения энергообмена в ишемизированных нейронах со снижением аэробного энергообмена, метаболизма АТФ, утилизации кислорода, глюкозы. Патологические процессы, протекающие в нервных волокнах при невропатиях, требуют коррекции вазоактивными препаратами. С целью улучшения процессов микроциркуляции и активизации процессов обмена и гликолиза у пациентов с туннельными невропатиями применяются кавинтон, галидор, трентал, инстенон.
Инстенон — комбинированный препарат нейропротекторного действия, включающий вазоактивный агент из группы пуриновых производных, влияющий на состояние восходящей ретикулярной формации и корково-подкорковые взаимоотношения, а также процессы тканевого дыхания в условиях гипоксии, физиологические механизмы ауторегуляции церебрального и системного кровотока. При невропатиях инстенон применяют внутривенно капельно 2 мл в 200 мл физиологического раствора, в течение 2 ч, 5–10 процедур на курс. Затем продолжается пероральный прием инстенона форте по 1 таблетке 3 раза в день в течение месяца. При невропатиях с симпатологическим синдромом показано применение инстенона по 2 мл внутримышечно 1 раз в сутки в течение 10 дней. При компрессионно-ишемических (туннельных) невропатиях используется аналогичная методика. Это способствует улучшению микроциркуляции и метаболизма в ишемизированном нерве. Особенно хороший эффект отмечается при сочетанном применении актовегина (капельно) и инстенона (внутримышечные инъекции или пероральное применение).
Галидор (бенциклана фумарат) — препарат, имеющий широкий спектр действия, что обусловлено блокадой фосфодиэстеразы, антисеротониновым эффектом, кальциевым антагонизмом. Галидор назначается в суточной дозе 400 мг в течение 10–14 дней.
Трентал (пентоксифиллин) применяют по 400 мг 2–3 раза в сутки внутрь или 100–300 мг внутривенно капельно в 250 мл физиологического раствора.
Назначение комбинированных препаратов, включающих большие дозы витамина В, противовоспалительных средств и гормонов, нецелесообразно.
Средствами первого ряда для снятия болевого синдрома остаются НПВП. Основной механизм действия НПВП — ингибирование циклооксигеназы (ЦОГ-1, ЦОГ-2) — ключевого фермента каскада метаболизма арахидоновой кислоты, приводящего к синтезу простагландинов, простациклинов и тромбоксанов. В связи с тем, что метаболизм ЦОГ играет главную роль в индукции боли в очаге воспаления и передаче ноцицептивной импульсации в спинной мозг, НПВП широко используются в неврологической практике. Имеются данные о том, что их принимают 300 млн пациентов (Г. Я. Шварц, 2002).
Все противовоспалительные средства оказывают собственно противовоспалительное, анальгезирующее и жаропонижающее действие, способны тормозить миграцию нейтрофилов в очаг воспаления и агрегацию тромбоцитов, а также активно связываться с белками сыворотки крови. Различия в действии НПВП носят количественный характер (Г. Я. Шварц, 2002), но именно они обусловливают выраженность терапевтического воздействия, переносимость и вероятность развития побочных эффектов у больных. Высокая гастротоксичность НПВП, коррелирующая с выраженностью их саногенетического действия, связана с неизбирательным ингибированием обеих изоформ циклооксигеназы. В связи с этим для лечения выраженных болевых синдромов, в том числе длительного, необходимы препараты, обладающие противовоспалительным и анальгезирующим действиями при минимальных гастротоксических реакциях. Наиболее известное и эффективное лекарственное средство из этой группы — ксефокам (лорноксикам).
Ксефокам — препарат с выраженным антиангинальным действием, которое достигается за счет сочетания противовоспалительного и сильного обезболивающего эффектов. Он является на сегодняшний день одним из наиболее эффективных и безопасных современных анальгетиков, что подтверждено клиническими исследованиями. Эффективность перорального применения по схеме: 1-й день — 16 и 8 мг; 2–4-й дни — 8 мг 2 раза в день, 5-й день — 8 мг/сут — при острых болях в спине достоверно доказана. Анальгетический эффект в дозе 2–16 мг 2 раза в сутки в несколько раз выше, чем у напраксена. При туннельных невропатиях рекомендуется использование препарата в дозе 16–32 мг. Курс лечения составляет не менее 5 дней при одноразовой ежедневной процедуре. Рекомендуется применение препарата ксефокам для лечения синдрома грушевидной мышцы по следующей методике: утром — внутримышечно 8 мг, вечером — 8–16 мг внутрь, в течение 5–10 дней, что позволяет добиться быстрого и точного воздействия на очаг воспаления при полном обезболивании с минимальным риском развития побочных реакций. Возможно проведение регионарных внутримышечных блокад в паравертебральную область по 8 мг на 4 мл 5% раствора глюкозы ежедневно в течение 3–8 дней. Симптоматическая терапия — метод выбора для купирования алгических проявлений. Наиболее часто для лечения туннельных невропатий используются лечебные блокады с анестетиками. Стойкий болевой синдром длительностью более 3 нед свидетельствует о хронизации процесса. Хроническая боль — сложная терапевтическая проблема, требующая индивидуального подхода.
В первую очередь необходимо исключить другие причины возникновения боли, после чего целесообразно назначение антидепрессантов.
М. В. Путилина, доктор медицинских наук, профессор
РГМУ, Москва




