при какой температуре плавится ртуть
О ртути
Ртуть: общие понятия
Консультация оперативного дежурного: +7(812)309-13-43
Химические свойства ртути
Ртуть – единственный из всех существующих в природе металлов, который остается жидким при комнатной температуре. В этих условиях на воздухе она не окисляется, в воде и щелочах не растворяется. Растворяется в холодной азотной кислоте и нагретой концентрированной серной. В обычных условиях активно испаряется, и скорость этого процесса прямо пропорциональна температуре и площади поверхности испарения. Пары ртути не имеют ни запаха, ни цвета, обнаружить их в воздухе можно только с помощью специальных приборов
Физические свойства ртути
Для ртути характерны низкая вязкость и высокое поверхностное натяжение. Эти свойства становятся причиной двух негативных с точки зрения ртутного загрязнения среды процессов:
Пары ртути отличает очень высокая летучесть, и слой воды или иной жидкости не представляет для них реальной преграды. То же самое можно сказать и о многих строительных материалах, таких как бетон, кирпич, лакокрасочное покрытие, линолеум или плитка. Ртутные пары равномерно пропитывают их на всю толщину, а также легко сорбируются из воздуха деревом, коврами и тканями. При повышении температуры или при механическом воздействии происходит обратная десорбция ртути в воздух помещения.
Чистая металлическая ртуть хорошо растворяет многие металлы, снижая тем самым прочность металлических конструкций, и образует непрочные соединения как с неорганическими, так и с органическими веществами.
Воздействие ртути на человека и животных
Основные пути попадания ртути в организм – это вдыхание ее паров с воздухом либо употребление с пищей или водой. Организм человека выводит не более 20% попавшей в него ртути, и она накапливается в почках и мозге, поражает плод, если женщина беременна, содержится в крови и грудном молоке. При концентрации паров ртути более 0,1 мг/м3 наступает острое отравление, признаки которого:
Следствием длительного воздействия малых доз ртути является хроническое отравление, которое может проявиться с задержкой на несколько лет. Все это время в организме накапливаются необратимые нарушения с такими внешними признаками:
Мнение эксперта:
Алена Парецкая, врач — педиатр
Пролитая ртуть: как с ней бороться
Существуют как природные (месторождения), так и техногенные (места добычи, горнорудные и предприятия цветной металлургии, специальные полигоны-хранилища, отходы сжигания нефтепродуктов и т. д.) источники ртути, загрязняющей воздух, воду и почву. Бытовые и производственные помещения загрязняются ртутью при неправильной эксплуатации ртутных приборов и устройств, таких как термометры, манометры, выпрямители электрического тока. Статистика утверждает, что 80% всех работ МЧС в Санкт-Петербурге источники паров ртути. Если не принимать во внимание злоумышленные проливы ртути, то наиболее частая причина их существования – разбитый ртутный термометр и преступно халатное отношение к последствиям этого события
Ликвидация розлива ртути: +7(812)309-13-43
ОЧЕНЬ ВАЖНО!
Если у Вас в семье есть ребёнок, заранее объясните ему, что если он нечаянно
разобьёт термометр, его никто не будет за это ругать. В противном случае ваше чадо, испугавшись наказания за разбитый градусник, спрячет его остатки куда-нибудь под кровать или шкаф и ничего Вам не скажет – в итоге вся Ваша семья долгое время будет дышать ядовитыми парами ртути.
При прохождении теста нужно помнить: Предельно допустимая концентрация ртути 300нг/м3
Основные свойства ртути и температура плавления
Температура плавления ртути характеризует момент перехода металла из твердого состояния в жидкость. Свойства живого серебра (argentum vivum в переводе с латинского) расширяют границы применения металла в разных сферах производства с учетом мер безопасности, связанных с его использованием.
Распространенность в природе
В земной коре концентрация химического элемента низкая. Ртутные рудные минералы содержат до 2,5% живого серебра. Это отличает их от других пород. В основном меркурий находится в рассеянной форме, и лишь часть находится в месторождениях.
В магматических породах долевое содержание живого серебра равно между собой, а в осадочных толщах крупные концентрации металла сосредоточены в глинистых минералах. Воды Мирового океана содержат 0,1 мкг/л меркурия.
Высокая степень ионизации определяет особенности металла:
Химический элемент присутствует в составе сульфидных минералов (сфалерит, реальгар). Этот металл является индикатором месторождений ртути и скрытых рудных тел. В поверхностных условиях живое серебро и киноварь не растворяются в воде, но при наличии серной кислоты, озона способствует увеличению показателя растворимости минералов.
Меркурий обладает отличными сорбционными свойствами. В природе существует около 20 минералов, содержащих этот металл, но промышленная добыча производится на месторождениях киновари.
Одно из крупнейших месторождений находится в Испании. Технология производства металла предусматривает обжиг киновари с последующей конденсацией и сбором паров ртути.
Физические и химические свойства живого серебра
Ртуть (меркурий) имеет уникальные химические и физические особенности, что позволяет ее применять в различных сферах. Но в то же время ее испарения опасны для человека. Как уже упоминалось, ее называют живым серебром, она по цвету напоминает лунный металл.
Меркурий обладает переходными свойствами, при комнатной температуре он остается в жидком состоянии. Живое серебро легко образует с другими материалами твердые и жидкие сплавы (амальгамы). Наиболее популярными являются соединения золота и серебра.
Химический элемент является диамагнетиком, и в случае необходимости собрать его магнитом невозможно. Он неплохо проводит ток, поэтому в свое время его применяли при изготовлении реле и выключателей.
Плотность живого серебра при нормальных условиях составляет 13,5 г/см³. Этот химический элемент обладает устойчивостью в сухом воздухе, окисляется только при нагревании выше +300°C. После длительного хранения на открытом воздухе на поверхности образуется пленка из оксидов компонентов, содержащихся в основном материале в качестве примесей.
При нагревании вступает в реакцию с кислородом, образуя оксид красного цвета. Металл малоактивный, не реагирует с растворами кислот, но растворяется в царской водке. При нагревании в серной кислоте образует сульфат ртути.
Сферы использования живого серебра
Ртуть применяется для изготовления точных измерительных приборов для определения температуры и давления. Сегодня в электрохимическом производстве широко используются ртутные выпрямители тока.
В медицинской отрасли для проведения профилактических работ в качестве источников ультрафиолетового спектра применяются ртутные (газоразрядные) лампы, всем известные градусники для измерения температуры тела содержат этот химический элемент.
В связи с тем, что меркурий токсичен, его не используют для изготовления медицинских препаратов. Хотя до середины 70-х годов ее активно применяли для производства мази от педикулеза.
Измерительные приборы для низкотемпературных условий содержат амальгаму таллия, которая в отличие от чистой ртути застывает при температуре – 60°C. Сочетание 2 токсичных металлов значительно расширяет границы использования.
За рубежом кипящую ртуть используют в качестве охладителя. Ее преимущество поддерживать постоянную температуру позволяет интенсивно отводить тепло от пространства катализатора. Для увеличения коэффициента отдачи в ртуть добавляют натрий для образования амальгамы.
С целью размягчения кадмия, олова и серебра меркурий используют в стоматологии при изготовлении пломб. Раньше ее применяли для золочения деталей часов и ювелирных изделий, а амальгамы золота и серебра использовались при производстве зеркал.
Живое серебро применяется в качестве катода для извлечения ряда активных компонентов электролитическим путем, а также для переработки вторичного алюминия.
Существуют технологии извлечения золота из россыпей с использованием свойства химического элемента образовывать амальгаму с благородным металлом. Этот метод был широко распространен в Индии, где в местах предполагаемого скопления золота проделывали специальные углубления, в которые заливали металлическую ртуть. Через некоторое время вытаскивали амальгаму, и путем выпаривания извлекали золото.
В нефтеперерабатывающей промышленности для регулировки температурных процессов используют пары ртути. В сельском хозяйстве ее используют для подготовки семян к посеву.
С давних времен и сегодня соли меркурия используют при изготовлении фетра, дублении кожи в качестве катализатора органического синтеза.
В прошлом ртуть не считалась вредным веществом, ее применяли для исцеления от недугов. В Средневековье алхимики использовали меркурий в поисках философского камня и превращения ее в золото.
Ртуть опасна для человека, она токсична и даже в ничтожных концентрациях плохо влияет на иммунную систему, почки, глаза, кожу и пищеварительный тракт.
Кипение и плавление металла
Технология физико-химических исследований при условиях высоких температур рассматривает давление плавления металла при разных температурах. Точность опытов обеспечивает применение на практике свойств химического элемента № 80.
Для измерения температуры выше +360°C пользуются термопарами или специальными термометрами, в которых пространство надо ртутью заполнено газом. С целью повышения температуры кипения металла в капилляр надо ртутью закачивают азот. При давлении 30 атмосфер температурный градиент увеличивается до +600°C.
Такого типа термометры требуют постепенного нагрева. Нижним пределом такого измерительного прибора является температура перехода живого серебра в твердое состояние.
Теплоемкость металла с увеличением температуры последовательно уменьшается и после определенного порога температурного градиента начинает медленно расти. Это свойство и жидкое состояние роднит ртуть с водой.
Ртуть
(молярная масса)
(первый электрон)
Содержание
История
Ртуть известна с древних времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и её соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий. Но принадлежность ртути к металлам была доказана только трудами Ломоносова и Брауна, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.
Происхождение названия
Нахождение в природе
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.
В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe2(SO4)3, озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa2S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями.
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7. В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg4Cl.
Месторождения
Ртуть считается редким металлом.
Одно из крупнейших в мире ртутных месторождений находится в Испании (Альмаден). Известны месторождения ртути на Кавказе (Дагестан, Армения), в Таджикистане, Словении, Киргизии (Хайдаркан — Айдаркен), Донбассе (Горловка, Никитовский ртутный комбинат).
В России находятся 23 месторождения ртути, промышленные запасы составляют 15,6 тыс. тонн (на 2002 год), из них крупнейшие разведаны на Чукотке — Западно-Палянское и Тамватнейское.
В окружающей среде
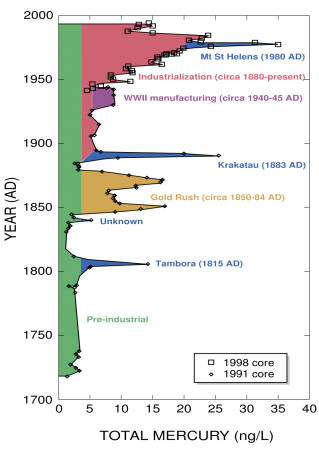
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограммов на 1 кубический дециметр льда. Природные источники, такие, как вулканы, составляют примерно половину всех выбросов атмосферной ртути. Причиной появления остальной половины является деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля (главным образом в тепловых электростанциях) — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6,8 %, производство цемента — 6,4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1,4 %, ртути (в основном для батареек) — 1,1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Изотопы
Природная ртуть состоит из смеси 7 стабильных изотопов: 196 Hg (распространённость 0,155 %), 198 Hg (10,04 %), 199 Hg (16,94 %), 200 Hg (23,14 %), 201 Hg (13,17 %), 202 Hg (29,74 %), 204 Hg (6,82 %). Искусственным путём получены радиоактивные изотопы ртути с массовыми числами 171—210.
Получение
Ртуть получают обжигом киновари (сульфида ртути II) или металлотермическим методом:
HgS + O2 ⟶ Hg + SO2↑ HgS + Fe ⟶ FeS↓ + Hg
Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании. В Новое время с ним стала конкурировать Идрия во владениях Габсбургов (современная Словения). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов. В 2012 г. ЮНЕСКО объявило промышленную инфраструктуру Альмадена и Идрии памятником Всемирного наследия человечества.
В надписях во дворце древнеперсидских царей Ахеменидов (VI—IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски.
Ртуть – особенности, сферы применения и чем опасен жидкий металл
История этого вещества накрепко связана со средневековыми алхимиками и китайскими даосами, искавшими эликсир (или пилюли) бессмертия. Ртуть есть в каждом доме, хотя весьма опасна.
Что представляет собой
Ртуть – элемент периодической системы Менделеева №80. Международное обозначение – Hydrargyrum (Hg).
Относится к металлам переходного типа. То есть сочетает характеристики жидкого и твердого вещества.

В стандартных условиях это массивная серебристо-белая жидкость с металлическим блеском.
Ртуть – единственный из металлов и один из двух химических элементов (второй – бром), при стандартных условиях представляющих собой жидкую субстанцию.
По составу металл ртуть – это конгломерат из семи стабильных изотопов. Еще четыре десятка радиоактивных изотопов созданы человеком.
История
В ртути обнаруживается примесь серебра и золота. Наверное, поэтому европейские алхимики эпохи Средневековья сделали ее одним из компонентов процедуры Великого Делания. То есть превращения простых металлов в золото либо серебро.
Древний мир
Ртуть как жидкое серебро упоминается Теофрастом и Аристотелем. Описана технология получения металла древними греками путем нагрева киновари с углем.
Однако на Востоке она была известна с XV века до нашей эры как один из семи священных металлов. Египтяне и китайцы также получали ее из киновари. Это был исходник для получения «пилюль бессмертия».
Россия, Европа
Научные опыты с веществом датируются серединой 18 века. Шведский химик Георг Брандт выделил чистую ртуть и описал процесс. Спустя 24 года российские ученые Михаил Ломоносов и Иосиф Браун получили твердое вещество. Попутно выявили свойства, присущие металлу (электропроводность в любом виде, ковкость).
Сегодня, как и во времена алхимиков, ртуть маркируется символом планеты Меркурий.
Название
История латинских названий ртути связана с представлениями европейцев об этом металле:
Славянские корни термина «ртуть» восходят к слову «руда». Оно обозначало все красное – цвет, кровь, краску.
Красным цветом наделена киноварь – природное соединение, из которого получали ртуть. Ее добывали на землях, заселенных восточными славянами (Донбасс).
Физико-химические характеристики
Главная особенность ртути, обусловленная структурой атома, – запредельный потенциал ионизации.
Отсюда свойства вещества:
В отличие от других «собратьев», ртуть плавится при отрицательной температуре: −38°С.
| Свойства атома | |
|---|---|
| Название, символ, номер | Ртуть / Hydrargyrum (Hg), 80 |
| Атомная масса (молярная масса) | 200,592(3) а. е. м. (г/моль) |
| Электронная конфигурация | [Xe] 4f14 5d10 6s2 |
| Радиус атома | 157 пм |
| Химические свойства | |
| Ковалентный радиус | 149 пм |
| Радиус иона | (+2e) 110 (+1e) 127 пм |
| Электроотрицательность | 2,00 (шкала Полинга) |
| Электродный потенциал | Hg←Hg2+ 0,854 В |
| Степени окисления | +2, +1 |
| Энергия ионизации (первый электрон) | 1 006,0 (10,43) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 13,546 (20 °C) г/см³ |
| Температура плавления | 234,32 K (-38,83 °C) |
| Температура кипения | 629,88 K (356,73 °C) |
| Уд. теплота плавления | 2,295 кДж/моль |
| Уд. теплота испарения | 58,5 кДж/моль |
| Молярная теплоёмкость | 27,98 Дж/(K·моль) |
| Молярный объём | 14,81 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | ромбоэдрическая |
| Параметры решётки | ahex=3,464 сhex=6,708 Å |
| Отношение c/a | 1,94 |
| Температура Дебая | 100,00 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 8,3 Вт/(м·К) |
| Номер CAS | 7439-97-6 |
Поэтому классифицируется как легкоплавкий металл.
Плотность ртути при нормальных условиях — 13 546 кг/м3, при других температурах — в таблице:
| Температура в °С | Плотность (ρ), 103 кг/м3 | Температура в °С | Плотность (ρ), 103 кг/м3 |
| 0 | 13,5950 | 50 | 13,4725 |
| 5 | 13,5827 | 55 | 13,4601 |
| 10 | 13,5704 | 60 | 13,4480 |
| 15 | 13,5580 | 65 | 13,4358 |
| 20 | 13,5457 | 70 | 13,4237 |
| 25 | 13,5335 | 75 | 13,4116 |
| 30 | 13,5212 | 80 | 13,3995 |
| 35 | 13,5090 | 90 | 13,3753 |
| 40 | 13,4967 | 100 | 13,3514 |
| 45 | 13,4845 | 300 | 12,875 |
Технология получения
Способы получения ртути не изменились со времен Средневековья. На предприятиях все так же обжигают киноварь (то есть сульфид ртути).
Месторождения, добыча
Ртутные месторождения планеты исчисляются поштучно:
В природе выявлено два десятка ртутных минералов, однако промышленный интерес представляет только киноварь (сульфид с содержанием ртути 86%). Иногда рентабельна добыча самородной ртути и шватцита (до 17%).
Присутствие в природе
Почти всегда вещество представлено в виде руды. Самые богатые ртутные руды содержат до 2,5% ртути.
Наиболее богаты ртутью породы осадочного происхождения (особенно глинистые сланцы) – до 200 мг/т. Вдвое беднее продукты вулканизма.
Каждая тонна земной коры содержит 0,83 г ртути. Каждый литр вод Мирового океана – 0,1 мкг.
Пары ртути ядовиты. Их выброс в атмосферу – «заслуга» вулканов и человека в равной мере. Люди создают такие осадки, эксплуатируя ТЭЦ, добывая золото, выплавляя цветные металлы, производя цемент, соду, утилизируя мусор.
Где используется
Традиционная сфера применения жидкого металла – термометры всех видов и назначения. Это и домашние градусники для измерения температуры тела, и высокоточные аппараты для специальных целей. Например, барометры и манометры.
Мы и сегодня измеряем атмосферное давление миллиметрами ртутного столба.
Без ртути невозможна работа серьезных отраслей.

Промышленный комплекс
Металл и его соединения применяются промышленниками и военными:
Исследуется потенциал ртутно-цезиевых сплавов как материала ионных двигателей.
Ртутные соединения применялись при выделке фетра. Это было опасно для здоровья работников, отсюда, вероятно, пошли легенды о «сумасшедшем шляпнике».
Другие сферы
До середины ХХ века ртутные соединения использовались медициной как материал зубных пломб, слабительное, антисептики, препарат для изничтожения вшей и лечения сифилиса.
Сегодня ртуть закачивают лишь в термометры (по 2 г), добавляют микродозами в вакцины.
Польза ртути для аграриев – пестициды и предпосевная протрава семян.
Предостережение
Даже микродозы ртути при попадании в организм способны сделать человека инвалидом:
Ртуть и все ее соединения отнесены к первому классу опасности. Безопасной дозы для человека не существует.
Содержание вещества регулируется санитарными нормами. Предельно допустимые концентрации в населенных пунктах или жилых помещениях – 0,0003 мг на кубометр.
Если разбился градусник
Если домашний градусник разбился, действовать нужно осторожно:
Наиболее опасны пары: ртуть начинается испаряться даже при комнатной температуре.
Шарики испаряются быстро. Поэтому демеркуризацию (очистку пространства от ртути) нужно проводить не мешкая.