при какой температуре разрушается хлор
При какой температуре испаряется хлор из воды?
Но не в этом дело. Хлор из воды можно удалить с помощью фильтра с активированным углём. Однако, что делать, если фильтра нет? Можно, конечно, купить. А если нет?
Итак, если налить воду в банку и, прикрыв крышкой, поставить отстаиваться на денёк-другой, то хлор из воды улетучится.
Не всё так просто, как казалось бы. При повышении температуры повышается реакционная способность хлора. И он начинает образовывать различные хлорорганические соединения, связываясь с молекулами органических веществ. Что получается в результате такого соединения? Правильно, яды. Трихлорметаны и прочие хлорорганические соединения.
При каких температурах они образовываются? Судя по статьям, которые я просмотрел, температура синтеза хлорорганических соединений находится в широком диапазоне, от 0 до 70 градусов Цельсия (с катализатором). Также есть упоминания о реакциях синтеза при больших температурах, до 1000 градусов.
Более подробных данных я не нашёл. Так что точно указать нужную температуру сложно. Однако, можно сделать такой вывод: испаряется хлор из воды при любой температуре. С повышением температуры скорость испарения увеличивается.
Одновременно увеличивается вероятность образования хлорорганических соединений. При температуре ниже 70 градусов Цельсия для образования хлорорганических соединений требуется катализатор (вещество, ускоряющее реакцию).
Соответственно, в обычной воде этого катализатора нет. Так что до температуры 70 градусов можно спать спокойно (теоретически).
При какой температуре разрушается хлорофилл
Получить выполненную работу или консультацию специалиста по вашему
учебному проекту
Хлорофилл.Зеленая окраска овощей (щавель, шпинат, салат, зеленый горошек и др.) и плодов ( крыжовника, винограда, ренклода) обусловлена присутствием в них хлорофилла. Имеется две разновидности хлорофилла: сине-зеленый и желто-зеленый. От соотношения этих разновидностей и зависят оттенки в окраске зеленых овощей.
( C32 H30 ON4 Mg) ∙ (COOCH3) ∙ (COOC20 H39) ; сине-зеленый хлорофилл
( C32 H28 O2 N4 Mg) ∙ (COOCH3) ∙ (COOC20 H39) ; желто-зеленый
Основу молекулы хлорофилла составляет сложное циклическое соединение (порфиновое ядро), связанное с ионом магния. При действии кислот хлорофилл теряет магний и переходит в бурое вещество – феофитин:
В зеленых овощах хлорофилл содержится в протоплазме в виде круглых или чечевицеобразных хлоропластов. В них он соединен с белками и липоидами. В сырых овощах хлоропласты защищены от действия кислот слоем протоплазмы.
Содержание хлорофилла в различных растительных продуктах, имеющих зеленую окраску, колеблется от 90 до 210 мг%. Хлорофилл дает с водой коллоидные растворы. Он хорошо растворяется в жире, его растворителях и водном спирте.
Хлорофилл используют в кулинарной практике при оформлении кондитерских изделий и для подкраски некоторых сладких блюд. Зеленые овощи и плоды утрачивают при варке нормальную окраску в результате взаимодействия хлорофилла с кислотами, содержащимися в клеточном соке. В сырых продуктах кислоты клеточного сока не. имеют доступа к хлорофиллу, находящемуся в протоплазме, вследствие полупроницаем ости ее кожистого слоя. свертывание белков в процессе варки, обусловливающее, с одной стороны разрушение кожистого слоя, а с другой – разрыв части связей между хлорофиллом и белком, делает возможным вступление хлорофилла в реакцию с кислотами клеточного сока.
Чем дальше продолжается нагревание, тем сильнее изменяется цвет. Чтобы цвет зеленых овощей лучше сохранялся, их следует варить, как можно быстрее и в большом количестве воды (3-4 л на 1кг) в открытой посуде при сильном кипении.
Так, щавель, содержащий Н2С2О4 и КНС2О4
В количестве 0,6-0,9 %, считая на кислую щавелево-калиевую соль, всегда значительно изменяет свой цвет при варке.
Варка зеленых овощей в жесткой воде способствует сохранению цвета, поскольку карбонаты щелочно – земельных металлов Са и Mg могут нейтрализовать некоторую часть кислот и кислых солей клеточного сока. Если вода, в которой варятся овощи, содержит ионы Fe, Sn, Al, Cu, то имеет место изменение окраски феофитина. Fe дает коричневую окраску, Sn и Аl сероватую, а Cu – устойчивую ярко-зеленую.
Цвет зеленых овощей хорошо сохраняется при варке их в слабом растворе соды. При этом происходит нейтрализация кислот и кислых солей клеточного сока, и создается щелочная среда за счет некоторого избытка соды в растворе.
Варка в щелочной среде вызывает омыление хлорофилла с образованием натриевой соли двухосновной кислоты, метилового спирта и фитола.
Необходимо указать, что даже при очень точной дозировке, исключающей ухудшение вкусовых качеств, ни медные соли, ни соду не следует применять для сохранения окраски зеленых овощей, так как это влечет за собой разрушение витамина С.
Если вам нужна помощь в написании работы, то рекомендуем обратиться к
профессионалам. Более 70 000 авторов готовы помочь вам прямо сейчас. Бесплатные
корректировки и доработки. Узнайте стоимость своей работы.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 октября 2020; проверки требует 1 правка.
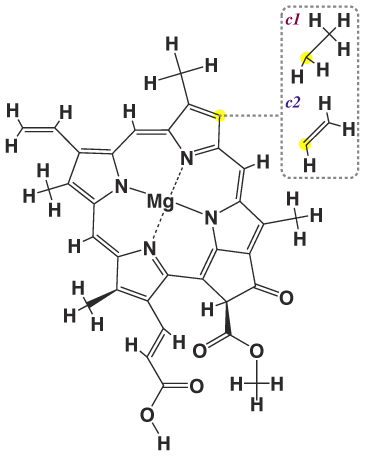
Строение хлорофилла c1 и c2
Хлорофи́лл (от греч. χλωρός, «зелёный» и φύλλον, «лист») — зелёный пигмент, окрашивающий хлоропласты растений в зелёный цвет. При его участии происходит фотосинтез. По химическому строению хлорофиллы — магниевые комплексы различных тетрапирролов. Хлорофиллы имеют порфириновое строение и близки гему.
Хлорофилл зарегистрирован в качестве пищевой добавки Е140.
История открытия[править | править код]
В 1817 году Жозеф Бьенеме Каванту и Пьер Жозеф Пеллетье выделили из листьев растений зелёный пигмент, который они назвали хлорофиллом[1]. В 1900-х годах Михаил Цвет[2] и Рихард Вильштеттер независимо обнаружили, что хлорофилл состоит из нескольких компонентов. Вильтштеттер очистил и кристаллизовал два компонента хлорофилла, названные им хлорофиллами а и b и установил брутто-формулу хлорофилла а. В 1915 году за исследования хлорофилла ему была вручена Нобелевская премия. В 1940 Ханс Фишер, получивший в 1930 Нобелевскую премию за открытие структуры гема, установил химическую структуру хлорофилла a. Его синтез был впервые осуществлен в 1960 Робертом Вудвордом[3], а в 1967 была окончательно установлена его стереохимическая структура[4].
В природе[править | править код]
Цвет листвы фотосинтезирующих растений обусловлен высокой концентрацией хлорофилла
Хлорофилл присутствует во всех фотосинтезирующих организмах — высших растениях, водорослях, синезелёных водорослях (цианобактериях), фотоавтотрофных простейших (протистах) и бактериях.
Некоторые высшие растения, наоборот, лишены хлорофилла (как, например, петров крест).
Синтез[править | править код]
Синтезирован Робертом Вудвордом в 1960 году.
Синтез включает в себя 15 реакций, которые можно разделить на 3 этапа. Исходными веществами для синтеза хлорофилла являются глицин и ацетат. На первом этапе образуется аминолевулиновая кислота. На втором этапе происходит синтез одной молекулы протопорфирина из четырёх пиррольных колец. Третий этап представляет собой образование и превращение магнийпорфиринов.
Свойства и функция при фотосинтезе[править | править код]
В процессе фотосинтеза молекула хлорофилла претерпевает изменения, поглощая световую энергию, которая затем используется в фотохимической реакции взаимодействия углекислого газа и воды с образованием органических веществ (как правило, углеводов):
После передачи поглощенной энергии молекула хлорофилла возвращается в исходное состояние.
Хотя максимум непрерывного спектра солнечного излучения расположен в «зелёной» области 550 нм (где находится и максимум чувствительности глаза), поглощается хлорофиллом преимущественно синий, частично — красный свет из солнечного спектра (чем и обуславливается зелёный цвет отражённого света).
Растения могут использовать и свет с теми длинами волн, которые слабо поглощаются хлорофиллом. Энергию фотонов при этом улавливают другие фотосинтетические пигменты, которые затем передают энергию хлорофиллу. Этим объясняется разнообразие окраски растений (и других фотосинтезирующих организмов) и её зависимость от спектрального состава падающего света.
Химическая структура[править | править код]
Хлорофиллы можно рассматривать как производные протопорфирина — порфирина с двумя карбоксильными заместителями (свободными или этерифицированными). Так, хлорофилл a имеет карбоксиметиловую группу при С10, фитоловый эфир пропионовой кислоты — при С7. Удаление магния, легко достигаемое мягкой кислотной обработкой, дает продукт, известный как феофитин. Гидролиз фитоловой эфирной связи хлорофилла приводит к образованию хлорофиллида (хлорофиллид, лишенный атома металла, известен как феофорбид a).
Все эти соединения интенсивно окрашены и сильно флуоресцируют, исключая те случаи, когда они растворены в органических растворителях в строго безводных условиях. Они имеют характерные спектры поглощения, пригодные для качественного и количественного определения состава пигментов. Для этой же цели часто используются также данные о растворимости этих соединений в соляной кислоте, в частности для определения наличия или отсутствия этерифицированных спиртов. Хлороводородное число определяется как концентрация HCl (%, масс./об.), при которой из равного объёма эфирного раствора пигмента экстрагируется 2/3 общего количества пигмента. «Фазовый тест» — окрашивание зоны раздела фаз — проводят, подслаивая под эфирный раствор хлорофилла равный объём 30%-го раствора KOH в MeOH. В интерфазе должно образовываться окрашенное кольцо. С помощью тонкослойной хроматографии можно быстро определять хлорофиллы в сырых экстрактах.
Хлорофиллы неустойчивы на свету; они могут окисляться до алломерных хлорофиллов на воздухе в метанольном или этанольном растворе.
Хлорофиллы образуют комплексы с белками in vivo и могут быть выделены в таком виде. В составе комплексов их спектры поглощения значительно отличаются от спектров свободных хлорофиллов в органических растворителях.
Хлорофиллы можно получить в виде кристаллов. Добавление H2O или Ca2+ к органическому растворителю способствует кристаллизации.
| Хлорофилл a | Хлорофилл b | Хлорофилл c1 | Хлорофилл c2 | Хлорофилл d | Хлорофилл f | |
|---|---|---|---|---|---|---|
| Формула | C55H72O5N4Mg | C55H70O6N4Mg | C35H30O5N4Mg | C35H28O5N4Mg | C54H70O6N4Mg | C55H70O6N4Mg |
| C2 группа | -CH3 | -CH3 | -CH3 | -CH3 | -CH3 | -CHO |
| C3 группа | -CH=CH2 | -CH=CH2 | -CH=CH2 | -CH=CH2 | -CHO | -CH=CH2 |
| C7 группа | -CH3 | -CHO | -CH3 | -CH3 | -CH3 | -CH3 |
| C8 группа | -CH2CH3 | -CH2CH3 | -CH2CH3 | -CH=CH2 | -CH2CH3 | -CH2CH3 |
| C17 группа | -CH2CH2COO-Phytyl | -CH2CH2COO-Phytyl | -CH=CHCOOH | -CH=CHCOOH | -CH2CH2COO-Phytyl | -CH2CH2COO-Phytyl |
| C17-C18 связь | Одинарная | Одинарная | Двойная | Двойная | Одинарная | Одинарная |
| Распространение | Везде | Большинство наземных растений | Некоторые водоросли | Некоторые водоросли | Цианобактерии | Цианобактерии |
Общая структура хлорофилла a, b и d
Структура хлорофилла c1, c2
Структура хлорофилла f
Оптический спектр поглощения хлорофиллов a (голубой) и b (красный)
Хроматограмма зелёного пигмента растений
Применение[править | править код]
Хлорофилл находит применение как пищевая добавка (регистрационный номер в европейском реестре E140), однако при хранении в этанольном растворе, особенно в кислой среде, неустойчив, приобретает грязно-коричнево-зеленый оттенок, и не может использоваться как натуральный краситель. Нерастворимость нативного хлорофилла в воде также ограничивает его применение в качестве натурального пищевого красителя. Но хлорофилл вполне успешно используется в качестве натуральной замены синтетических красителей при изготовлении кондитерских изделий.[источник не указан 3185 дней]
Производное хлорофилла — хлофиллин медный комплекс (тринатриевая соль) получил распространение в качестве пищевого красителя (Регистрационный номер в европейском реестре E141). В отличие от нативного хлорофилла, медный комплекс устойчив в кислой среде, сохраняет изумрудно-зеленый цвет при длительном хранении и растворим в воде и водно-спиртовых растворах. Американская (USP) и Европейская (EP) фармакопеи относят хлорофиллид меди к пищевым красителям, однако вводят лимит на концентрацию свободной и связанной меди (тяжелый металл).
Хлорофилл придаёт листьям зелёный цвет и поглощает свет при фотосинтезе
В клетках эукариотов хлорофилл обычно находится в хлоропластах
Карта распределения хлорофилла по поверхности мирового океана в период с 1998 по 2006 по данным спутникового прибора SeaWiFS
Примечания[править | править код]
Ссылки[править | править код]
Трубоогневая сушка. Технология трубоогневой сушки табака нашла широкое распространение в первой половине XX века практически во всех странах, производящих табак. При трубоогневой сушке табака весь процесс, начиная с томления, проходит в сушилке.
Внешним показателем протекающего процесса томления является окраска табачных листьев, которая из зеленой постепенно переходит в желтую. Изменение окраски листьев взаимосвязано с изменением содержания хлорофилла. На скорость изменения хлорофилла при томлении табака влияют степень зрелости табака и температурно-влажностный режим томления. Чем выше температура томления, тем быстрее разрушается хлорофилл. При температуре воздуха ниже 16°С и выше 45°С он практически не разрушается.
Скорость разрушения хлорофилла зависит и от относительной влажности воздуха в период томления. При влажности ниже 40% и выше 95% хлорофилл не разрушается. Установлено, что до тех пор, пока табак не потеряет 20-25% исходного содержания воды, содержание хлорофилла в табаке остается практически неизменным. Наиболее интенсивно хлорофилл разрушается при влажности табака 75%, т.е. после того, как табак потерял не менее 40-50% первоначальной своей массы.
Скорость разрушения хлорофилла резко возрастает при сушке табака, убранного на более поздних стадиях созревания листьев. Так, уборка листьев в состоянии полной технической зрелости позволяет увеличить скорость разрушения хлорофилла в 2,5-3 раза по сравнению со скоростью разрушения его в листьях, убранных в состоянии «надзелень».
Хлорофилл при томлении разрушается независимо от распада остальных элементов состава табака, но его разрушение идет параллельно гидролизу крахмала и белков.
Распад хлорофилла при томлении табака связан с динамикой потери воды листьями. Установлено, что коэффициент корреляции между скоростью потери воды табаком при томлении и распадом в листьях хлорофилла колеблется у разных сортов от 0,57 до 0,95. Исчезновение зеленой окраски означает окончание томления табака.
Успех искусственной сушки табака в значительной мере определяется подбором однородной партии, так как листья разных ботанических сортов, разных ломок, разной степени зрелости ведут себя при сушке по-разному. Например, незрелые листья процесс томления проходят медленно и неравномерно, медленно высыхают и дают сырье зеленой или бурой окраски, низкого товарного качества. Перезрелые листья быстро высыхают, но сырье получается только с окраской темных тонов (красное, коричневое).
В связи с вышеизложенным партия табака, поступающая для трубоогневой сушки, должна подбираться в соответствии со следующими требованиями:
– табак необходимо убирать с поля в состоянии технической и полной технической зрелости;
– партия табака должна быть однородной по зрелости, одного ботанического сорта и одной ломки; в загружаемую партию должен входить табак одного срока ломки (в пределах суток);
– необходимо следить за сохранностью листьев табака, избегая повреждения ткани;
– партия для сушки по возможности подбирается с участков, имеющих одинаковые почвенные условия.
Из внешних факторов, определяющих скорость и направленность процесса томления табака, наиболее существенными являются температура и относительная влажность воздуха. Наиболее благоприятная температура для фазы томления 32-38°С. Обычно томление начинают при температуре 28-32°С.
В связи с тем, что томление табака – процесс изменения состава табачных листьев, сохраняющих жизнеспособность, температуру воздуха в этой фазе необходимо повышать постепенно, а максимальное значение ее не должно превышать 38-39°С. В начале томления табака относительная влажность воздуха должна поддерживаться на уровне 75-80%.
Такое сочетание температуры и влажности воздуха в сушилке необходимо поддерживать до появления желтой окраски у верхушки листа.
Пожелтевшую часть листа следует подсушивать, в то же время надо сохранять жизнедеятельное состояние остальной части пластинки листа. Поэтому температуру воздуха в сушилке в этот период поднимают до 37-38°С и, усилив вентиляцию, снижают влажность воздуха до 65-70%.
Таким изменением режима усиливают отбор влаги из табака, чтобы к концу томления снизить ее содержание до минимума и облегчить последующую фиксацию окраски вытомленных листьев. Фаза фиксации – наиболее ответственный этап при трубоогневой сушке.
С момента пожелтения листовой пластинки на 1/3 приступают к проведению фазы фиксации окраски, для чего медленно повышают температуру воздуха при одновременном снижении его относительной влажности.
Медленное повышение температуры от 38°С ведется с таким расчетом, чтобы через 12-16 часов она достигла 45°С; относительную влажность воздуха снижают за этот же период времени до 40-45%. Такие условия поддерживают до подсыхания большей части пластинки листа. К этому времени почти исчезает зелень, оставшаяся у средней жилки и основания листа.
После подсыхания большей части листа приступают к проведению третьей фазы процесса трубоогневой сушки – сугике листовых пластинок. Для этого температуру воздуха в сушилке повышают до 48-50°С и поддерживают на этом уровне до окончательного высыхания всей листовой пластинки. Далее приступают к последней фазе – досушке средних жилок, которые у основания листа долгое время остаются сырыми. Для ускорения высушивания жилки температуру воздуха необходимо повысить до 60°С, а чтобы лучше сохранялось тепло в сушилке, следует полностью закрыть вентиляцию. Влажность воздуха в сушилке при этой температуре уже невысокая и при закрытой вентиляции легко удаляется из сушилки.
Продолжительность сушки средних жилок зависит в основном от температуры воздуха (табл. 8).
Влияние температуры на продолжительность сушки
средних жилок листьев табака сорта Юбилейный (в час)
Данные таблицы свидетельствуют о том, что за счет повышения температуры воздуха с 60 до 120°С продолжительность сушки средних жилок снижается в 7-12 раз. Однако, в трубоогневых сушилках в период досушки средних жилок повышать температуру выше 60°С не рекомендуется, так как при более высоких температурах возрастает пожароопасность, а также ухудшаются технологические свойства табака.
Сушка считается закопченной, если средняя жилка па всем ее протяжении от основания до верхушки становится хрупкой и ломается при перегибе ее пальцами.
Нормально идущий процесс трубоогневой сушки, включая и фазу томления, длится для табаков: мелколистных – 65-70, среднелистных – 76-80, крупнолистных – 120-144 часов.
Если на сушку поступил крупнолистный табак, выращеный на тяжелых почвах, из которого трудно отобрать влагу, то в этом случае проводят предварительное подвяливание. После загрузки табака в сушилку температуру воздуха повышают до 40-42°С при полной вентиляции и поддерживают такой режим 5-6 часов. При этом табачные листья энергично испаряют влагу, перегрева листьев не происходит.
Если табак по истечении указанного времени еще сохраняет много
зелени, то температуру воздуха в сушилке снижают до 33-35°С и, закрыв вентиляцию, продолжают томление обычным путем.
Сырье трубоогневой сушки имеет обычно светло-желтую окраску и обладает специфическим вкусом, отличным от вкуса сырья естественных способов сушки.
Приведенная технология трубоогневой сушки является примерной. В каждом отдельном случае в зависимости от свойств табака могут быть отклонения в режиме как по температуре, так и по относительной влажности воздуха.
Выше был описан полный цикл сушки с искусственным подогревом воздуха, когда в сушилке проводят все операции: томление, фиксацию цвета, сушку листовой пластинки и досушку средних жилок. Но такой способ сушки в период уборки табака применять во всех районах табаководства нецелесообразно, за исключением тех случаев, когда хозяйство производит сырье искусственного способа сушки.
Полную сушку табака в искусственных условиях целесообразно применять при высушивании верхних ломок, убранных при неблагоприятных погодных условиях.
В странах СНГ трубоогневым способом издавна сушат табак на Кубани, в Крыму, в Закавказье. Этот способ успешно применяется в Молдове, особенно во вторую половину сушильного сезона для средних и верхних ломок.
Наибольшее распространение для сушки крупнолистных сортов табака получил способ сушки в плотной в массе при помощи сушилок типа «Балк-Кюринг», работающих по типу трубоогневой сушки. Здесь листья размещаются на иглах кассет и применяется принудительная вентиляция, что позволяет значительно увеличить концентрацию листьев табака в сушильной установке и повысить ее производительность. Применение этого способа дает возможность снизить трудовые затраты (в 5-10 раз) за счет исключения процесса нанизывания листьев табака на шнуры. В Молдове, однако, за последнее десятилетие таким способом табак практически не сушат из-за высоких удельных энергозатрат.
Основой сушки в плотной массе является воздействие на массу табачных листьев мощным воздушным потоком, который пронизывает межлиственные пространства с одинаковой силой. Сушильный агент (воздух) подогревается в теплообменниках и поступает через
перфорированный пол в камеру, пронизывая трехъяруснук табачных листьев. «Продувка» массы листьев мощным потоком как раз и является отличительной особенностью сушки табака в плотной массе, позволяющей значительно увеличить степень заполнения сушильного пространства табаком.
Зима придет, потом настанет лето, и снова хлорофилл зазеленит
Подножие каждой пищевой пирамиды, существующей в самых различных климатических условиях – тундра и саванна, коралловый риф и дно океана, держат на своих плечах скромные труженики биосферы – фотосинтетические организмы-продуценты, которым помогает производить первичную биомассу такая замечательная молекула, как хлорофилл.
Несмотря на то, что мы знаем про процесс фотосинтеза практически все, что про него можно знать, он все равно кажется волшебством – превращение энергии фотонов в энергию химическую, превращение солнечного света в пищу. Древние, поклонявшиеся Солнцу, как богу, дающему жизнь всему на земле, должны были бы внести в свой пантеон и еще одного маленького (не по значению, а по размерам) бога-хлорофилла – все могущество Солнца без этой молекулы было бы потрачено впустую и только благодаря хлорофиллу все существующее многообразие форм жизни появилось практически из ничего – воздуха, воды и света.
Фотосинтез – уникальный физико-химический процесс, осуществляемый на Земле всеми зелеными растениями и некоторыми бактериями и обеспечивающий преобразование электромагнитной энергии солнечных лучей в энергию химических связей различных органических соединений. Основа фотосинтеза — последовательная цепь окислительно-восстановительных реакций с образованием углеводов и выделением кислорода (строго говоря – для самих-то растений выделение кислорода представляет собой процесс побочный или факультативный – главное, ради чего растение занимается фотосинтезом – синтез углеводов, которые затем участвуют в других обменных процессах).
Разработанное природой средство, позволяющее конвертировать световую энергию в химическую, представляет собой порфириновый цикл с длинными боковыми цепями. В центре порфиринового цикла, гемовой структурной единицы, практически не отличающейся от уже упоминавшегося замечательного вещества с гемом – гемоглобина, находится ион магния. Строение порфирина, а точнее – чередование одинарных и двойных связей, обеспечивает поглощение электромагнитного излучения с определенной длиной волны, из-за чего как сами порфирины, так и их комплексы с металлами зачастую имеют характерную окраску.
Боковые цепи хлорофилла производят «тонкую настройку» длины поглощающейся волны света. Существует несколько типов хлорофилла, различающихся именно строением боковых цепей, причем у высших растений, как правило, в листе одновременно два типа хлорофилла (a и b) – присутствие сразу двух видов молекул хлорофилла способствует тому, что растения более эффективно поглощают энергию Солнца.
Другие фотосинтезирующие водоросли и фотосинтезирующие бактерии имеют иной набор пигментов. Например, бурые и диатомовые водоросли, криптомонады и динофлагелляты содержат хлорофиллы a и c, красные водоросли — хлорофиллы а и d. Следует отметить, что реальность существования хлорофилла d в красных водорослях оспаривается некоторыми исследователями, которые полагают, что он является продуктом деградации хлорофилла а. В настоящее время достоверно установлено, что хлорофилл d — основной пигмент некоторых фотосинтезирующих прокариотов. Среди прокариотов цианобактерии (сине-зеленые водоросли) содержат только хлорофилл a, прохлорофитные бактерии — хлорофиллы a, b или c.
Другие бактерии содержат аналоги хлорофилла — бактериохлорофиллы, которые локализованы в хлоросомах и хроматофорах. Известны бактериохлорофиллы а, b, c, d, e и g. Основу молекулы всех хлорофиллов составляет магниевый комплекс порфиринового макроцикла, к которому присоединен высокомолекулярный спирт, обладающий гидрофобными свойствами, который придает хлорофиллам способность встраиваться в липидный слой фотосинтетических мембран.
Тем не менее, главная роль в улавливании и трансформации солнечной энергии в биосфере принадлежит хлорофиллам а и b. Если хлорофилл а имеет обычную зеленую окраску, оттенок хлорофилла b в большей степени уходит в желтизну. Хлорофиллы поглощают синюю и красную компоненты солнечного света, а привычная нам зелень летней листвы (или зимней хвои) – это те цвета, которые остаются после поглощения листьями красноты и синевы.
Весной и летом хлорофилл дает листве свою зеленую окраску, но каждую осень лиственные деревья и кустарники меняют цвет своей листвы, на несколько недель принося в скучную серую осень буйство всей палитры желтых и красных красок. До настоящего времени считалось, что цвета золотой осени обуславливаются наличием в листьях каротиноидов и флавоноидов. Основным объяснением появления желто-красной окраски листьев было следующее – флавоноиды и каротиноиды содержатся и в зеленых листьях, однако их окраска замаскирована зеленой окраской хлорофилла, который разрушается осенью, прекращая маскировать желтый и красный цвета. Однако это лишь часть химических процессов, протекающих в листьях осенью.
Процесс распада хлорофилла долгое время оставался загадкой для исследователей. Около двух десятков лет назад из листвы были выделены продукты разложения хлорофилла, которые оказались бесцветными, что лишний раз добавило исследователям уверенности в том, что хлорофилл, разлагаясь, только делает видимыми другие окрашенные соединения. Тем не менее, недавно было выяснено, что обнаруженные ранее продукты распада хлорофилла, считавшиеся окончательными, могут окисляться с образованием интенсивно-желтых соединений. Строение желтых продуктов распада хлорофилла похоже на структуру билирубина, природного соединения, предохраняющего клетки от повреждения.
С разложением хлорофилла связан и следующий интересный факт – зреющие бананы при облучении ультрафиолетом флуоресцируют с испусканием интенсивно синего цвета. Это синее свечение связано с разрушением хлорофилла, протекающим при созревании бананов. В результате такого расщепления бесцветные, но флуоресцирующие продукты распада хлорофилла концентрируются в банановой кожуре.
Привычный вид бананов обусловлен наличием каротиноидов, которые обуславливают желтую окраску банановой кожуры при нормальном освещении. При облучении ультрафиолетом созревающие бананы выглядят интенсивно синими, причем окраска не зависит от того, каким образом происходит созревание – естественным или подстегивается с помощью газообразного этилена. Зеленые незрелые бананы не флуоресцируют. Интенсивность флуоресценции определяется степенью распада хлорофилла и увеличивается по мере созревания.
В растениях хлорофиллы локализованы в мембранах клеточных органоидов – хлоропластов, именно там молекулы хлорофилла могут улавливать энергию входящих фотонов, в результате воздействия фотонов хлорофиллы переходят в возбужденное состояние. Расположение молекул хлорофилла в хлоропластах способствует тому, что энергия может передаваться между соседними молекулами, фокусируясь и умножаясь таким образом, что в итоге от молекулы хлорофилла отрывается электрон, который затем участвует в целой цепочке других химических превращений.
Реакции с участием оторвавшегося электрона создают достаточную энергию для синтеза углеводов из углекислого газа. При этом молекула хлорофилла, потерявшая электрон, регенерирует свое состояние за счет отрыва электрона от воды, в процессе окисления воды в качестве побочного продукта фотосинтеза образуется кислород, и никогда еще побочный продукт не был таким полезным.
Общий процесс фотосинтеза появился в результате эволюции миллиарды лет назад в зеленых бактериях, а затем закрепился как свойство клеток многоклеточных растений. По сути дела каждый хлоропласт представляет собой реликтовый остаток древней бактерии, «взятой в заложники» современным растением из-за своей удачной способности.
Вопрос о дате «начала» фотосинтеза является одним из главных среди тех, которые обсуждаются в связи с происхождением жизни на Земле. Считается, что до появления фотосинтеза атмосфера обладала «восстановительными» свойствами – состояла из метана, аммиака и сероводорода. Фотосинтез вызвал первую «экологическую катастрофу», приведшую к исчезновению практически всех не кислорододышащих форм жизни.
Наиболее старое ископаемое свидетельство существования фотосинтетических бактерий позволяло предположить, что они появились в экологической системе Земли около 2,7 миллиардов лет назад. Тем не менее, недавно полученные при изучении скальных пород свидетельства позволяют предположить, что бактерии, способные к фотосинтезу уже существовали на Земле 3,46 миллиарда лет назад.
В настоящее время исследователи пытаются приручить процесс фотосинтеза и использовать его идею для использования солнечной энергии – к таким попыткам использовать энергию Солнца в солнечных батареях, системах фотокаталитического получения водорода – топлива будущего, из воды, а также другие системы, позволяющие проводить конверсию солнечной энергии в энергию химическую. Сравнительно недавно было обнаружено, что наносистемы из оксида титана под воздействием солнечного света могут расщеплять воду на водород и кислород
В пищевой промышленности хлорофилл используется в качестве красителя (добавка Е-141), именно хлорофилл придает зеленую окраску абсенту, который, по легендам вдохновлял Дега, Уайлда, Ван Гога и Хемингуэя, во время творчества которых этот напиток был настолько популярен, что в определенных кругах счастливые часы называли «зелеными часами». Вообще-то и у автора этих строк были свои связанные с абсентом и неделей счастья зеленые часы в Питере, а точнее в его пригороде.
Итак, хлорофилл представляет собой не только замечательное вещество, которое дало нам всем жизнь, но и неиссякаемый источник вдохновения как для химиков и инженеров, так и для поэтов, писателей и художников.