при какой температуре воздух становится жидким
Физические свойства кислорода
Где бы мы ни находились, нас всюду окружает кислород воздуха.
Почему же мы не замечаем и не чувствуем его? Кислород, азот, аргон и другие газы, входящие в состав воздуха, бесцветны и не имеют ни запаха, ни вкуса. Газообразный воздух нельзя ни видеть, ни ощущать.
Воздух из газообразного состояния можно перевести в жидкое. Одновременно с основной массой воздуха — азотом — в жидкое состояние перейдут кислород и большинство других газов, входящих в его состав.
Чтобы газообразный кислород превратить в жидкость, его нужно сжать до 50 атмосфер и охладить до —119°.
Жидкий кислород можно получить и при атмосферном давлении, но для этого нужно газообразный кислород охладить до температуры —183°. При более сильном охлаждении, до температуры —220°, жидкий кислород затвердевает и превращается в снегообразную массу.
Если на некоторое время в жидкий кислород поместить кусочек резины, она потеряет свою эластичность и под ударом разлетится на мелкие части.
Такую же хрупкость приобретает и цинковая пластинка, охлажденная в жидком кислороде до температуры —183°. Жидкая ртуть при такой температуре превращается в твердую массу, которую можно ковать, как свинец, а свинец приобретает способность звенеть, как бронзовый колокольчик.
Жидкий кислород имеет голубоватый цвет. Его можно легко переливать из сосуда в сосуд. При переливании жидкий кислород «парит». Но это не пары кислорода, а пары воды. Жидкий кислород, испаряясь, поглощает много тепла из окружающего воздуха. Воздух сильно охлаждается, и влага, находящаяся в воздухе, конденсируется, образуя туман. Этот туман и создает впечатление пара, исходящего из самой жидкости.
Температура кипения жидкого кислорода равна —183°.
Если фарфоровый стакан с жидким кислородом вынести зимой на мороз 30—40°, он будет кипеть более бурно, чем вода на самом сильном огне газовой плиты.
При комнатной температуре испарение жидкого кислорода идет еще энергичнее, и он быстро переходит в газообразное состояние.
Чтобы использовать жидкий кислород, его необходимо сохранить. Как же заставить эту бурно кипящую жидкость не так быстро испаряться?
Для этого служат специальные сосуды, в которых легко удается «укротить» эту быстро испаряющуюся жидкость.
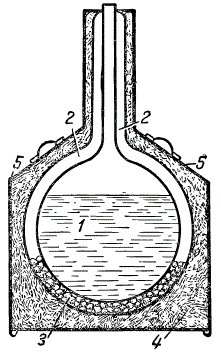
Стеклянный сосуд для хранения небольшого количества жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — поверхности, посеребренные внутри.
Сосуд для хранения жидкого кислорода представляет собой цилиндр с двойными стенками. Внутренние стороны стенок обычно покрывают тонким слоем серебра. Воздух между стенками сосуда выкачивается.
Разреженные газы плохо проводят тепло, а зеркальная поверхность серебра хорошо отражает его. Таким образом, жидкий кислород, который находится в сосуде, изолирован от внешнего тепла, что обеспечивает сохранение жидкого кислорода в течение одних-двух суток.
При испарении жидкого кислорода объем его увеличивается почти в 800 раз. Из кубического сантиметра жидкого кислорода образуется около 800 кубических сантиметров газообразного.
Хранить жидкий кислород в закрытых сосудах опасно: внутри сосуда может образоваться большое давление, приводящее к взрыву. Поэтому сосуды для хранения жидкого кислорода сверху открыты. Воздух, находящийся над жидкостью, сильно охлаждается и предохраняет кислород от наружного тепла, замедляя дальнейшее испарение.
Для перевозки небольших количеств жидкого кислорода используют металлические емкостью 15—25 литров.
Металлические сосуды состоят из двух шаров или цилиндров, вставленных друг в друга. Внутренний шар или цилиндр имеет высокое и узкое горло, через которое сосуд заполняется жидким кислородом. Горло всегда остается открытым. Из пространства между стенками сосуда воздух выкачан, и создан высокий вакуум, то есть сильное разрежение.
Металлический сосуд для перевозки жидкого кислорода: 1 — жидкий кислород; 2 — разреженное пространство; 3 — силикагель; 4 — теплоизоляционный материал; 5 — железный цилиндр.
Чтобы поддержать высокий вакуум, часть пространства между стенками заполняется силикагелем, способным при низкой температуре поглощать количество газа в сотни раз больше своего собственного объема. Если через стенки или через места спайки со временем просочится небольшая часть воздуха, он поглотится силикагелем и разрежение не уменьшится. Высокий вакуум обеспечивает постоянную изоляцию сосуда от внешнего тепла и дает возможность в течение двух и более суток сохранять в нем жидкий кислород. Такие сосуды обычно помещают в железные цилиндры.
Пространство между сосудом и наружным цилиндром заполняют теплоизоляционным материалом. Для переноски на наружном цилиндре имеются ручки.
Большие количества жидкого кислорода перевозятся по железной дороге и автотранспортом в специальных цистернах или танках. Они хорошо изолированы от внешнего тепла. Емкость транспортных танков различна: от 1 тысячи до 10 тысяч литров. Цистерны, в которых жидкий кислород перевозят по железной дороге, вмещают до нескольких десятков тонн.
Жидкий кислород можно получить из жидкого воздуха, который образуется при низких температурах и высоком давлении.
Высокое давление создают в машинах, которые называются компрессорами. Их приводят в движение электродвигатели.
Источник: В. Медведовский. Кислород. Государственное Издательство Детской литературы Министерства Просвещения РСФСР. Ленинград. Москва. 1953
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
При какой температуре воздух становится жидким
3. Сжижение газов
Газы отличаются от жидких тел расстоянием между молекулами. Казалось бы поэтому, что для сжижения газа достаточно сблизить его молекулы, т. е. сильно сдавить газ. Однако оказалось, что это не так и что для превращения газа в жидкое состояние должна быть путем охлаждения газа снижена движущая (кинетическая) энергия молекул.
| Название газа | Плотность (воздуха = 1) | Вес 1 литра в г при 0°С и 760 мм | 1 кг газа = литрам газа | Уд. вес жидкого газа при темпер. 15°С вода = 1 (4°) | Давление паров жидкого газа при 150 атм | Точка кипения °С | Точка плавления °С | Критич. температура °С | Критич. давление атм |
| Азот | 0,9701 | 1,2542 | 789 | 0,7914 (-196°) | — | 196° | -211° | -147° | 34 |
| Аммиак | 0,5895 | 0,7621 | 1 312 | 0,6138 | 7,14 | -38,5° | -75° | -132° | 112 |
| Аргон | 1,379 | 1,782 | 561 | 1,212 (-186°) | — | -186° | -190° | -121° | 51 |
| Ацетилен | 0,8988 | 1,620 | 617 | 0,420 (10°) | 37,9 | -84° | -81° | 37° | 68 |
| Водород | 0,0697 | 0,0900 | 11 106 | 0,0763 (-253°) | — | -259° | -253° | -239° | 12 |
| Гелий | 0,1382 | 0,1787 | 5 596 | 0,122 (-269°) | — | -269° | -272° | -268° | 2 |
| Двуокись азота | 3,1812 | 4,1126 | 243 | 1,451 | 0,76 | 26° | 11° | 171° | 100 |
| Двуокись серы | 2,2131 | 2,8611 | 350 | 1,3964 | 2,72 | -10° | -79° | 157° | 78 |
| Двуокись углерода | 1,5201 | 1,9652 | 509 | 0,814 | 52,17 | -78° | -65° | 31,1° | 73 |
| Закись азота | 1,5229 | 1,9688 | 508 | 0,800 | 49,77 | -90° | -115° | 36° | 75 |
| Кислород | 1,1055 | 1,4292 | 700 | 0,106 (-183°) | — | -183° | -218° | -119° | 51 |
| Криптон | 2,868 | 3,654 | 274 | 2,16 (-152°) | — | -152° | -169° | -63° | 54 |
| Ксенон | 4,49 | 5,717 | 175 | 3,52 (107°) | — | -107° | -140° | 15° | 57 |
| Метан | 0,5539 | 0,7160 | 1 396 | 0,466 (-160°) | — | -160° | -184° | -96° | 50 |
| Метиламин | 1,0737 | 1,388 | 720 | 0,699 (-11°) | — | -6° | — | 155° | 72 |
| Неон | 0,695 | 0,9004 | 1 111 | 0,456 (-233°) | — | -233° | -253° | -228° | 27 |
| Окись углерода | 0,9673 | 1,2506 | 800 | 0,7676 (-184°) | — | -190° | -207° | -140° | 36 |
| Фосген | 3,4168 | 4,4172 | 227 | 1,392 | 1,35 | 8,2° | -118° | — | — |
| Хлор | 2,4494 | 3,1666 | 316 | 1,4273 | 5,75 | -33,6° | -102° | 146° | 94 |
| Хлористый метил | 1,7438 | 2,2543 | 443 | 0,917 (17°) | 4,10 | -24° | -104° | 142° | 73 |
| Хлористый этил | 2,2280 | 2,8804 | 347 | 0,921 (0°) | 1,09 | 12,5° | -143° | 182° | 54 |
| Этиламин | 1,558 | 2,0141 | 497 | 0,689 | 0,9 | 18° | -85° | 177° | 66 |
| Этилен | 0,9684 | 1,252 | 798 | 0,310 (6°) | 46 (6°) | -103° | -169° | 10° | 51 |
| Этан | 1,038 | 1,3421 | 746 | 0,466 | 32,3 | -84° | -171° | 35° | 45 |
Сжижение газов является в настоящее время важной отраслью химической промышленности. Так напр., сжижается воздух, и из него при помощи фракционированной дистилляции получается кислород, азот и редкие газы. Сжижается хлор и в жидком виде транспортируется в стальных баллонах на отбельные заводы. Жидкие сернистый ангидрит, аммиак и другие жидкие газы применяются в холодильных установках. Их действие заключается в том, что сильно сжатому компрессором и охлажденному газу представляется возможность сразу расшириться (в пространстве, из которого компрессором отсасывается воздух через так наз. редукционный клапан); в результате этого газ так сильно охлаждается, что превращается в жидкость (явление Джоуля-Томсона). Испарением жидкого газа охлаждается рассол (крепкий солевой раствор), который затем распределяется по помещениям, предназначенным для охлаждения.
Стальные баллоны необходимо оберегать от ударов (при транспортировке) и нельзя подвергать действию высокой температуры (оставлять на солнце или вблизи от отопительной установки или печи). У кислородных баллонов нарезки нужно смазывать не смазочным маслом, а глицерином.
При какой температуре воздух становится жидким
Жи́дкий кислоро́д (ЖК, жO2, LOX [1] ) — жидкость бледно-синего цвета, которая относится к сильным парамагнетикам. Является одним из четырёх агрегатных состояний кислорода. Жидкий кислород обладает плотностью 1,141 г/см³(1141 кг/м³) и имеет умеренно криогенные свойства с точкой замерзания 50,5 K (−222,65 °C) и точкой кипения 90,188 K (−182,96 °C).
Жидкий кислород активно используется в космической и газовой отраслях, при эксплуатации подводных лодок, широко используется в медицине. Обычно промышленное получение основывается на фракционной перегонке воздуха. Коэффициент расширения кислорода при смене жидкого агрегатного состояния на газообразное составляет 860:1 при 20 °C, что иногда используется в системах снабжения кислородом для дыхания в коммерческих и военных самолётах.
Содержание
Получение [ править | править код ]
Основным и практически неисчерпаемым источником получения жидкого кислорода является атмосферный воздух: производится сжижение воздуха и последующее разделение его на кислород и азот.
Физические особенности [ править | править код ]
Из-за своей криогенной природы жидкий кислород может вызвать хрупкость материалов, которые находятся с ним в соприкосновении.
Парамагнетические свойства [ править | править код ]
Химические свойства [ править | править код ]
Жидкий кислород также является очень мощным окислительным агентом: органическое вещество быстро сгорает в его среде с большим выделением тепла. Более того, некоторые из этих веществ, будучи пропитанными жидким кислородом имеют свойство непредсказуемо взрываться. Часто так ведут себя нефтепродукты, включая асфальт.
Применение [ править | править код ]
Компонент ракетного топлива [ править | править код ]
Жидкий кислород является широко распространённым окислительным компонентом ракетных топлив обычно в комбинации с жидким водородом или керосином. Его использование обусловлено высоким удельным импульсом, который получается при применении этого окислителя в ракетных двигателях. Кислород — самый дешевый из применяемых компонентов ракетных топлив. Первое использование имело место в германской БР Фау-2, позднее в американских БР «Редстоун» и РН «Атлас», а также в советской МБР Р-7. Жидкий кислород активно использовался в ранних МБР, но более поздние версии этих ракет его не используют из-за криогенной природы и необходимости регулярной дозаправки для компенсации выкипания окислителя, что затрудняет быстрый запуск. Многие современные ЖРД используют ЖК в качестве окислителя, например РД-180, RS-25.
Хранение и транспортировка [ править | править код ]
В качестве уплотнительных прокладочных материалов в системах с жидким кислородом применяются материалы, не теряющие эластичности при низких температурах: паронит, фторопласты, отожженные медь и алюминий.
Хранение и транспортировка больших количеств жидкого кислорода осуществляется в ёмкостях объёмом от нескольких десятков до 1500 м³ из нержавеющей стали, снабженных теплоизоляцией, а также в сосудах Дьюара. Наружный, защитный кожух теплоизоляции может выполняться и из углеродистой стали. Резервуары транспортных ёмкостей изготавливаются также из сплава АМц. Применение вакуумно-порошковой или экранно-вакуумной теплоизоляции позволяет снизить суточные потери кипящего продукта до уровня 0,1—0,5 % (в зависимости от размеров ёмкости) и скорость повышения температуры переохлажденного — до 0,4—0,5 К в сутки.
Транспортировка кипящего кислорода производится с открытым вентилем газосброса, а переохлажденного — при закрытом вентиле, с контролем давления не реже 2 раз в сутки; при повышении давления больше, чем на 0,02 МПа (изб.) вентиль открывается.
Хранение с жидким азотом [ править | править код ]
Жидкий азот имеет более низкую точку кипения 77 K (−196 °C) и устройства, которые содержат жидкий азот, могут конденсировать кислород из воздуха: когда большая часть азота испаряется из такого устройства возникает риск того, что остаток жидкого кислорода может сильно прореагировать с органическими материалами. С другой стороны, жидкий азот или жидкий воздух может оказаться насыщенным жидким кислородом, если оставить ёмкость на открытом воздухе — атмосферный кислород будет в ней растворяться, в то время как азот будет испаряться быстрее.
Общий характер высотного изменения температуры воздуха был предугадан Аристотелем.
Он делил атмосферу на три слоя, из которых прилегающий к Земле пригоден для жизни, следующий сильно охлаждён, а самый верхний, наоборот, сильно нагрет.
При достаточном охлаждении воздух переходит в жидкое состояние.
Жидкий воздух можно довольно долго сохранять в сосудах с двойными стенками, из пространства между которыми для уменьшения теплопередачи выкачан воздух. Подобные сосуды используются, например, в термосах.
Кислородный прибор с жидким воздухом
Лишь в 20-х годах ХIХ века, применяя значительные давления, удалось получить в жидком состоянии хлор, аммиак, диоксид углерода и ряд других веществ “газообразной природы”. Однако оставались ещё многие, в частности основные газы воздуха — кислород и азот, которые, несмотря на все усилия, не сжимались. На них перенесли то представление, которое раньше было общим, и стали считать их “постоянными” газами.
Только в 1877 г. впервые удалось получить в жидком состоянии одни из этих “постоянных” газов — кислород. Вслед за тем были сжиженны и все другие.
Здесь легко и интересно общаться. Присоединяйся!
Ссылка https://goo.gl/oeHYUv Будете поражены, насколько уникальным является этот шанс. Нас уже более 5 млн. человек. Проект не имеет аналогов в интернете, платит живые деньги (доллары). Мой скайп: wladimir_ska. Добавляйтесь в контакт, буду рад все объяснить и помочь добиться головокружительного успеха в свободное от работы время. Жду Вас!)

минус чего-то там за сотню, не помню
не только температура важна еще очень важна сила тяжести
здесь умных я и еще полтора головы)
В жарком климате при 80-ти градусах и выше.
кгда водух превращается в магму
при очень отрицательной! )
http://otvet.mail.ru/question/22352083
при обычном давлении азот превращается в жидкость при – 195 град. С
Воздух становится жидким при температуре около 80°К ( –190°C)
Общий характер высотного изменения температуры воздуха был предугадан Аристотелем.
Он делил атмосферу на три слоя, из которых прилегающий к Земле пригоден для жизни, следующий сильно охлаждён, а самый верхний, наоборот, сильно нагрет.
При достаточном охлаждении воздух переходит в жидкое состояние.
Жидкий воздух можно довольно долго сохранять в сосудах с двойными стенками, из пространства между которыми для уменьшения теплопередачи выкачан воздух. Подобные сосуды используются, например, в термосах.
Кислородный прибор с жидким воздухом
Лишь в 20-х годах ХIХ века, применяя значительные давления, удалось получить в жидком состоянии хлор, аммиак, диоксид углерода и ряд других веществ “газообразной природы”. Однако оставались ещё многие, в частности основные газы воздуха — кислород и азот, которые, несмотря на все усилия, не сжимались. На них перенесли то представление, которое раньше было общим, и стали считать их “постоянными” газами.
Только в 1877 г. впервые удалось получить в жидком состоянии одни из этих “постоянных” газов — кислород. Вслед за тем были сжиженны и все другие.
При какой температуре воздух становится жидким
при какой температуре воздух становится жидким? воздух температура
Воздух становится жидким при температуре около 80°К ( –190°C)
Общий характер высотного изменения температуры воздуха был предугадан Аристотелем.
Он делил атмосферу на три слоя, из которых прилегающий к Земле пригоден для жизни, следующий сильно охлаждён, а самый верхний, наоборот, сильно нагрет.
При достаточном охлаждении воздух переходит в жидкое состояние.
Жидкий воздух можно довольно долго сохранять в сосудах с двойными стенками, из пространства между которыми для уменьшения теплопередачи выкачан воздух. Подобные сосуды используются, например, в термосах.
Кислородный прибор с жидким воздухом
Лишь в 20-х годах ХIХ века, применяя значительные давления, удалось получить в жидком состоянии хлор, аммиак, диоксид углерода и ряд других веществ “газообразной природы”. Однако оставались ещё многие, в частности основные газы воздуха — кислород и азот, которые, несмотря на все усилия, не сжимались. На них перенесли то представление, которое раньше было общим, и стали считать их “постоянными” газами.
Только в 1877 г. впервые удалось получить в жидком состоянии одни из этих “постоянных” газов — кислород. Вслед за тем были сжиженны и все другие.
При какой температуре воздух становится жидким?
При какой температуре воздух становится жидким?
Как известно, воздух по своему составу неоднороден для различных температур, высот, давлений. Поэтому можно только говорить об усредненных значениях.
Воздух, это смесь газов. У каждого компонента воздуха свои свойства, поэтому говорить о жижком воздухе некорректно.
Но это не весь воздух, а только 0,03%
Если пренебречь величиной атмосферного давления, то средняя цифра температуры, при которой все составляющие воздуха превращаются в жидкость «-194» градуса по Цельсию.
Таких температур можно добиться только в лабораторных условиях.
Поэтому если мы говорим именно о воздухе, то особое внимание следует уделить критическим температурам (которые неразрывны с такими понятиями, как критическое давление и критический объем, т.е. не только температура имеет значение) кислорода и азота, их можно увидеть на картинке ниже:
Интересно, что жидкий воздух прекрасно хранится в специальных сосудах наподобие термоса, его стенки двойные, а из промежутка между этими стенками выкачивают воздух, чтобы снизить теплопередачу.
Воздух, это азот и кислород.
Температура при которой эта смесь становится жидкой минус 190-о градусов Цельсия.
Но при такой низкой температуре состав воздуха меняется, ибо тот же азот испаряется быстрей чем кислород, то есть через короткое время это уже будет не «классический» воздух.
Ну и конечно надо учитывать о каком давлении идёт речь (-190-о это обычное атмосферное давление).
Так как воздух в основном состоит из азота и кислорода, то нужно рассматривать свойства именно этих газов.
Средней темпиратурой, при которой происходит трансформация воздуха и всего всего что идет к нему в добавку, в атмосфере, является температура в интервале от 183 и до 195 граддусов по цельсию и это уже точно. Есть варианты, когда это может произойти и при менее низких температурах, но не факт, так как тут уже есть нюансы, которые говорят нам о том, какие вещества будут находится в атмосфере.
Наверное этот вопрос ранее изучали на предмете химии, но я лично не помню при какой температуре воздух становится жидким.
Жидкий воздух получают лабораторным путем.
При хранении состав жидкого воздуха значительно изменяется.
Нормы температуры воздуха в квартире существуют только во время отопительного сезона. Температуру воздуха замеряют на внутренней стене каждого помещения на расстоянии одного метра от наружной стены и полутора метров от пола.
Минимальная температура в помещениях : угловая комната +20 градусов, жилая комната +18 градусов, кухня +18 градусов, ванная комната +25 градусов.
Температура горячей воды из-под крана должна быть круглогодично не ниже 50 и не выше 70 градусов (САНПИН 2.1.2.1002-00).
Ту скорее обратный процесс. Чем ниже температура- тем снега больше. Вода в атмосфере замерзает и выпадает в виде осадков- снега. Если и дальше понижать температуру, то будут замерзать и другие газы и выпадать так же в виде снежинок или льдинок.
Но если, например, взять снег и принести в теплую комнату, то он конечно будет охлаждать там воздух, попутно тая. И чем больше вы принесете снега, тем больше охладите этот объем воздуха.
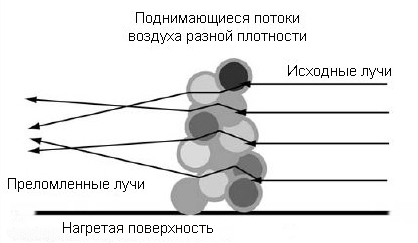
Природное явление марево проявляется в реальной жизни, когда изображения предметов кажутся искаженным из-за потоков воздуха, поднимающихся над нагретой поверхностью (огонь, асфальт, песок на пляже). С физической точки зрения мы наблюдаем эффект преломления. Аналогичный эффект наблюдается при опускании палки в воду, создается иллюзия, что по плоскости поверхности воды палка сломана, если смотреть сбоку.
Аналогичное происходит и в случае с маревом, нагретый воздух, менее плотный, чем окружающий создает границу преломления (холодный-горячий) по аналогии (воздух-вода). И начинает подниматься, на его место поступает холодный воздух. Возникает динамический процесс, зрительно воспринимаемый как марево.