при какой температуре железо становится газообразным
При какой температуре железо становится газообразным
Температура плавления химически чистого железа составляет 1539 о С. Технически чистое железо, полученное в результате окислительного рафинирования, содержит некоторое количество растворенного в металле кислорода. По этой причине температура его плавления понижается до 1530 о С.
Температура плавления стали всегда ниже температуры плавления железа в связи с наличием в ней примесей. Растворенные в железе металлы (Mn, Cr, Ni. Co, Mo, V и др.) понижают температуру плавления металла на 1 – 3 о С на 1% введенного элемента, а элементы из группы металлоидов (C, O, S, P и др.) на 30 – 80 о С.
На протяжении большей части общей продолжительности плавки температура плавления металла изменяется главным образом в результате изменения содержания углерода. При концентрации углерода 0,1 – 1,2%, которая характерна для доводки плавки в сталеплавильных агрегатах, температуру плавления металла с достаточной для практических целей точностью можно оценить из уравнения
Теплота плавления железа составляет 15200 Дж/моль или 271,7 кДж/кг.
Температура кипения железа в изданиях последних лет приводится равной 2735 о С. Однако, опубликованы результаты исследований, согласно которым температура кипения железа значительно выше (до 3230 о С).
Теплота испарения железа составляет 352,5 кДж/моль или 6300 кДж/кг.
Давление насыщенного пара железа (PFe, Па) можно оценить при помощи уравнения
где Т – температура металла, К.
Результаты расчета давления насыщенного пара железа при различных температурах, а также содержания пыли в окислительной газовой фазе над металлом (X, г/м 3 ) представлены в таблице 1.1.
Таблица 1.1 – Давление насыщенного пара железа и запыленность газов при разных температурах
Динамическая вязкость. Коэффициент динамической вязкости жидкости (
где F – сила взаимодействия двух движущихся слоев, Н;
S – площадь соприкосновения слоев, м 2 ;
Динамическая вязкость сплавов железа обычно изменяется в пределах 0,001 – 0,005 Па•с. Ее величина зависит от температуры и содержания примесей, главным образом углерода. При перегреве металла над температурой плавления выше 25 – 30 о С влияние температуры не существенно.
Кинематическая вязкость жидкости представляет собой скорость передачи импульса в потоке единичной массы. Ее величина определяется из уравнения
Удельная теплоемкость жидкого металла практически не зависит от температуры. В оценочных расчетах величину ее можно принимать равной 0,88 кДж/(кг•К) для чугуна и 0,84 кДж/(кг•К) для стали.
Поверхностное натяжение железа имеет максимальное значение при температуре около 1550 о С. В области более высоких и низких температур величина его уменьшается. Это отличает железо от большинства металлов, для которых характерно понижение поверхностного натяжения при повышении температуры.
Поверхностное натяжение жидких сплавов железа существенно меняется в зависимости от химического состава и температуры. Обычно оно изменяется в пределах 1000 – 1800 мДж/м 2 (рисунок 1.1).
Рисунок 1.1 – Влияние примесей на величину поверхностного натяжения сплавов железа
Растворимость. Весьма ограниченную растворимость в жидком и твердом железе имеют щелочные (Li, Na, K, Rb, Cs) и щелочноземельные (Mg, Ca, Ba, Sr) металлы. Кроме того практически нерастворимыми являются Ag, Cd и Bi.
К числу металлов, имеющих неограниченную растворимость в железе, относятся Mn, Ni, Co, Cu, Al, Sb, Ce и все редкоземельные металлы.
Ограниченной растворимостью в железе обладают Cr, V, Mo, W, Ti, Zr, Pb, Sn, Pt и др. Но при высоких температурах все металлы этой группы, кроме Pb и Sn, растворяются в расплавах железа в неограниченных количествах.
Железо: химические свойства и температура плавления

Железо и его свойства
Железо — это химический элемент, который в таблице Менделеева находится под номером 26. Это один из самых распространенных элементов во всей Солнечной системе. Согласно материалам исследований, в составе ядра Земли находится примерно 79−85% этого вещества. В земной коре его тоже присутствует большое количество, но оно уступает алюминию.
В чистом виде металл имеет белый цвет с чуть серебристым оттенком. Он пластичен, но имеющиеся в нем примеси могут определять его физические свойства. Реагирует на магнит.

Оксид железа — это основная форма, добыча которой осуществляется и которая находится в природе. Оксидное железо может располагаться в самой верхней части земной коры и быть составляющей осадочных образований.
Элемент, находящийся на двадцать шестом месте в таблице Менделеева, может иметь несколько степеней окисления. Именно они определяют его геохимическую особенность нахождения в определенной среде. В ядре Земли металл присутствует в нейтральной форме.
Добыча полезных ископаемых
Руд, в которых присутствует железо, существует несколько. Однако, в качестве сырья для производства железа в промышленности используют в основном следующие:
А также часто встречаются такие разновидности руды:
Существует еще минерал под названием мелантерит. Его используют преимущественно в фармацевтической промышленности. Из себя он представляет зелёного цвета хрупкие кристаллы, в которых присутствует стеклянный блеск. Из него производят лекарственные препараты, в составе которых имеется ферум.
Основным месторождением этого металла является Южная Америка, а именно Бразилия.
Плавление железа и необходимая температура
Точкой плавления металла называют такую минимальную температуру, при которой он переходит из твердого состояния в жидкое. При этом в объеме он практически остается неизменным.

Температура плавления железа весьма высока. Для технически чистого элемента она составляет +1539 °C. В этом веществе присутствует примесь — Сера, которую можно извлечь лишь в жидком виде. Без примесей чистый материал получают при электролизе солей металла.
Классификация металлов по температуре плавления
Разные металлы могут переходить в жидкое состояние при разной температуре. Вследствие этого выделяют определённую классификацию. Их делят следующим образом:
Единственный элемент, который при обычных условиях находится в жидком состоянии — это ртуть. Температура его плавления составляет минус 39 градусов и его пары являются ядовитыми, поэтому его используют только в лабораториях и закрытых ёмкостях.
Могут ли железо, ртуть и свинец стать газами
Мы привыкли воспринимать вещества и материалы по нахождению их в той или иной группе таблицы Менделеева. Причем, обычный человек с уверенностью может отличить лишь несколько семейств химических элементов: металлы, неметаллы и газы. На самом деле таких семейств насчитывается 10, некоторые из них имеют типичные, характерные для той или иной группы свойства, другие же являются переходными. Их характеризуют свойства нескольких семейств, и химики выделили их в отдельную побочную подгруппу.
Обычный человек скорее даже не станет заглядывать в периодическую таблицу, чтобы определить, к какому семейству относится вещество. Он будет оценивать качества по внешнему виду, запаху или на ощупь.
Мы видим мир снаружи
Мы встречаемся с соединениями и элементами на каждом шагу. Во время утечки природного газа чувствуется запах добавки, человек понимает, что помещение наполняет газ CH4. Покупка шариков перед праздником, сопровождается их закачкой гелием (He). Человек осознает, что перед ним находятся газы.

Во время приготовления пищи повара добавляют в блюда NaCl – пищевую соль. Наши бабушки, делая ремонт в домах, использовали для покраски стен белильную известь (CaOCl). Конечно, они растворяются в воде, но в нормальных условиях выглядят порошками и мы понимаем, что это неметаллы.
Металлы имеют прочную структуру, их невозможно помять, прогнуть. Достаточно вспомнить железный прут, бронзовую статую, свинцовую пулю. Есть, конечно, более податливые металлы — ртуть, медь, серебро, алюминий, натрий, рубидий. Они имеют металлический блеск, но обладают меньшей по сравнению с железом, свинцом, плотностью и могут деформироваться без особых усилий. Но и тут по внешнему виду можно определить, что предмет металлический. Мы привыкли так видеть окружающий мир, поэтому новые свойства привычных вещей могут ввести человека в ступор.
Химики видят вещества изнутри
Химики видят вещества с иной стороны. Они знают, что железо, ртуть и свинец, могут выглядеть иначе. В лабораторных условиях можно придать металлам газообразное состояние. Да, и даже тяжелые металлы, такие, как свинец и ртуть, могут летать.
Для этого используется специальное оборудование, в котором металлы закипают, превращаясь в газ. Ртуть закипает при 356,73°C, свинец при 1749°C, железо, при 2862°C. При этом происходит вполне стандартное кипение веществ со сменой кристаллической решетки и выходом пара наверх. После нормализации температурных условий пар оседает, превращаясь в капли металла.
Этим обусловлена ситуация, когда одежда металлургов на соответствующих предприятиях запачкана тончайшим слоем твердых веществ, так как при высоких температурах они превращаются в пар, а затем оседают.

Конечно, железо никогда не поднимется в воздух без особых условий, это удел иллюзионистов и фокусников. Но умелое обращение с земными «твердынями» доказывает, что за наукой стоит наше будущее.
Создавая новые материалы, изучая свойства уже существующих, специалисты с каждым открытием делают технологичней наш мир.
Может ли металл быть газом?
Да, металлы могут быть газами, в зависимости от того, насколько высока их температура кипения. Но действительно ли газообразные металлы считаются металлами?
Закройте на мгновение глаза и позвольте слову «металл» всплыть в вашей голове. А теперь ответьте: какой первый образ приходит вам на ум, когда вы думаете о «металле»?
Может ли металл быть газом?
Да, конечно! Хотя металлы обычно находятся в твердом состоянии при комнатной температуре (вероятно, поэтому мы ассоциируем слово «металл» с твердыми объектами), металлы также могут быть газами.
Дело в том, что состояния вещества универсальны: металл может быть твердым, жидким или газообразным. Но это состояние определяется на основе правильных условий температуры и давления.
Например, металл, скажем, свинец, имеет температуру кипения 1740 градусов по Цельсию. Теперь вы знаете, что свинец в своем «естественном состоянии» представляет собой твердое вещество. Но когда вы начнете его нагревать, он сначала превратится в жидкость при 327 градусах Цельсия, а если вы продолжите подавать больше тепла, он превратится в газ при 1740 градусах Цельсия.
Свинец превращается в пар при 1740 градусах Цельсия.
Но учтите, что пары ртути очень вредны. По данным Всемирной организации здравоохранения, «вдыхание паров ртути может оказывать вредное воздействие на нервную, пищеварительную и иммунную системы, легкие и почки и может быть фатальным. Неорганические соли ртути разъедают кожу, глаза и желудочно-кишечный тракт, а при попадании внутрь могут вызывать токсическое воздействие на почки«.
А теперь давайте обсудим еще один аспект этой саги о превращении металла в газ.
Остается ли металл металлом, когда он превращается в газ?
Мы установили, что металлы могут превращаться в газы, если их нагреть до точки кипения. Но если металл нагревается до точки кипения и становится газом, остается ли он металлом? Другими словами, может ли металл находиться в газообразном состоянии и при этом оставаться металлом?
Но почему металлы твердые? Что в них такого особенного, что делает их твердыми?
Почему металлы вообще твердые?
Металлы твердые при комнатной температуре из-за того, как их последовательные атомы упаковываются внутри.
Видите ли, вся материя состоит из атомов. Состояние вещества зависит от того, насколько близко или далеко друг от друга находятся эти атомы.
Если составляющие атомы вещества находятся далеко друг от друга, то это вещество будет существовать в виде газа при комнатной температуре. Атомы в жидком состоянии относительно ближе друг к другу, но в твердых телах атомы упакованы вместе в плотные кристаллы.
Из-за сильных сил, которые удерживают эти атомы близко друг к другу, твердые тела жесткие и имеют определенную форму и размер (в отличие от жидкости и газа).
Металлы твердые при комнатной температуре, потому что входящие в их состав атомы металлов упаковываются близко друг к другу, придавая им жесткий или «затвердевший» внешний вид. Это также является причиной того, что металлы имеют высокую температуру плавления и не существуют в жидком состоянии при комнатной температуре.
В целом, металлы могут превращаться в газ, но как только они превращаются в газ, они не сохраняют своих металлических свойств.
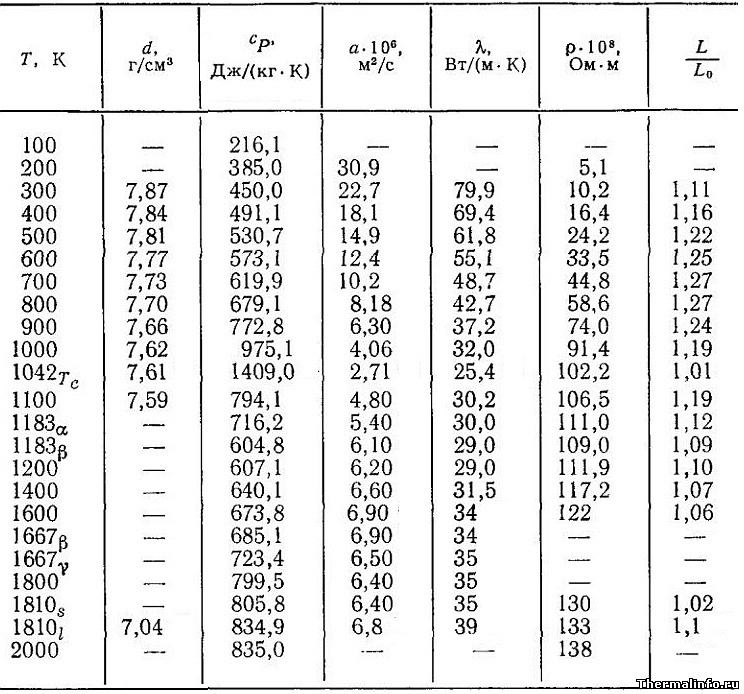
Плотность железа Fe, удельная теплоемкость, теплопроводность и другие его свойства

Свойства железа существенно зависят от температуры: при нагревании этого металла его плотность, теплопроводность и температуропроводность уменьшаются, а значение удельной теплоемкости железа растет.
Плотность железа равна 7870 кг/м 3 при комнатной температуре. При нагревании железа его плотность снижается. Поскольку железо является основным элементом в составе стали, то плотность железа определяет и значение плотности стали. Зависимость плотности железа от температуры слабая — при его нагревании плотность металла снижается и принимает минимальное значение 7040 кг/м 3 при температуре плавления, равной 1810 К или 1537°С.
Удельная теплоемкость железа, по данным таблицы, имеет значение 450 Дж/(кг·град) при температуре 27°С. В зависимости от структуры удельная теплоемкость твердого железа при увеличении температуры изменяется по-разному. По значениям в таблице видны характерный максимум теплоемкости железа вблизи Tc и скачки при структурных переходах и при плавлении.
Теплопроводность железа при комнатной температуре равна 80 Вт/(м·град). С ростом температуры теплопроводность железа снижается — она имеет отрицательный температурный коэффициент в области температуры 100-1042 К, а затем начинает слабо расти. Минимальное значение теплопроводности железа составляет 25,4 Вт/(м·град) вблизи точки Кюри. При β-γ переходе наблюдается слабое изменение теплопроводности, которое также имеет место и при γ-δ переходе.
Теплопроводность железа резко падает по мере увеличения количества примесей, особенно кремния и серы. Наивысшей теплопроводностью обладает очень чистое электролитическое железо — его теплопроводность при 27°С равна 95 Вт/(м·град).
Зависимость коэффициента теплопроводности железа от температуры также определяется степенью чистоты этого металла. Чем железо чище, тем выше его теплопроводность и тем больше по абсолютной величине она снижается с повышением температуры.