с какими металлами взаимодействует ртуть
Химия, Биология, подготовка к ГИА и ЕГЭ
Ртуть — элемент побочной подгруппы второй группы шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 80. Обозначается символом Hg (лат. Hydrargyrum). Простое вещество ртуть — переходный металл, при комнатной температуре представляет собой тяжёлую серебристо-белую жидкость, пары которой чрезвычайно ядовиты.
Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии
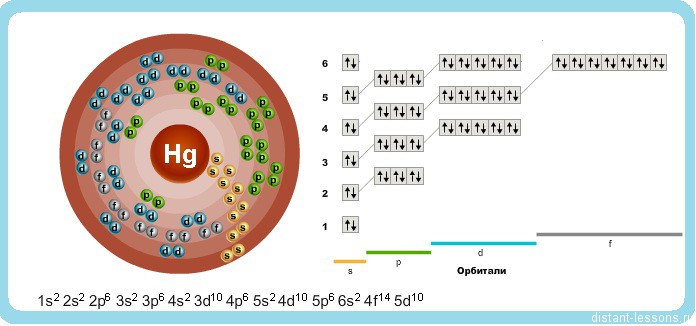
Исходя из электронного строения, можно сделать вывод, что для в соединениях ртуть будет проявлять степени окисления +2 и +1.
Физические свойства ртути:
Как видите, все вышеперечисленные свойства — характеристики металлического вещества, хотя и в жидком состоянии.
Химические свойства ртути:
1) Реакция с кислородом (при нагревании >300 ° С): 2Hg + O2 = 2HgO (красного цвета);
2) реагирует с водородом, но только с атомарным ( так же при нагревании): Hg + 2H = HgH2 — гидрид ртути;
3) C неметаллами ( при нагревании): Hg + S = HgS
4) Взаимодействие с кислотами: с кислотами-не окислителями не взаимодействует
В ряду активности металлов ртуть стоит после водорода, поэтому в реакциях с кислотами-окислителями водород не выделяется:
Как видно из реакции, чаще всего в соединениях ртуть проявляет степень окисления + 2, но +1 тоже встречается, причем в очень необычном виде:
Степень окисления
Соединения ртути
Оксид — не выделен;
Гидроксид — не выделен
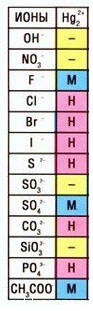
Кстати, таких соединений ртути (I) немало — смотрите таблицу растворимости:
Оксид — HgO (относят к слабым основным или даже амфотерным оксидам);Гидроксид — не выделен
Что касается соединений ртути (II), то не смотря на то, что простое вещество ртуть — металл, в веществах HgS (черные или красные кристаллы) и HgJ2 (желтые кристаллы) cвязь ковалентная.
Связь ртуть-углерод в органических соединениях ртути самая прочная из всех известных металл-органических связей
Соединения ртути чрезвычайно ядовиты, соответственно, как и большинство других ядов, их часто используют в медицине:
Ртуть — металл с удивительными свойствами
В нашем магазине продаются самые разнообразные 
Ртуть — химический элемент таблицы Менделеева, простое неорганическое вещество, металл. Известна человечеству уже более семи тысяч лет. Ее использовали в V в. до н.э. в Месопотамии, о ртути знали в Древнем Китае и на Ближнем Востоке. Ее получали простым обжигом киновари на кострах, а потом с ее помощью выплавляли золото и серебро.
Основные свойства
Обозначается символом Hg (гидраргирум, в переводе с греческого «жидкое серебро»). Это название элементу дали алхимики.
Ртути на планете не так уж и много, но она очень рассеяна: есть в воздухе, воде, в большинстве горных пород. Встречается в самородном виде в виде капель, но редко. Гораздо чаще — в составе минералов и глин. Входит в состав более 30 минералов, промышленное значение имеет киноварь (HgS). Получают ртуть сейчас гораздо более технологичным способом, чем в древности, но смысл процесса остался тот же: обжиг киновари.
С химической точки зрения

Легко при нормальных условиях реагирует с раствором перманганата калия в щелочи и с хлорсодержащими веществами. Это свойство используется для удаления разливов ртути. Опасный участок заливают хлорсодержащим отбеливателем типа «АСС», «Белизна» или хлорным железом.
Образует сплавы со многими металлами — амальгамы. К амальгамированию устойчивы железо, вольфрам, молибден, ванадий и некоторые другие металлы. Образует с металлами меркуриды — интерметаллические соединения.
Об опасности ртути
Ртуть относится к веществам 1-й группы опасности, 
Ртуть запрещено перевозить самолетами. И вовсе не потому, что она токсична. Все дело в том, что она легко растворяет алюминий и его сплавы. Случайное разлитие может привести к повреждению корпуса самолета.
Введение
История
Ртуть известна с древних времен. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом природной киновари. Древние греки и римляне использовали ртуть для очистки золота (амальгамирование), знали о токсичности самой ртути и её соединений, в частности сулемы. Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твердость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 г. Для представления элемента как у алхимиков, так и в нынешнее время используется символ планеты Меркурий. Но принадлежность ртути к металлам была доказана только трудами Ломоносова и Брауна, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства: ковкость, электропроводность и др.
Ртуть – вещество первого класса опасности. Является переходным металлом, представляющим собой серебристо-белую жидкость с тяжелой массой, пары которой очень ядовиты (в условиях привычной температуры жилых помещений).
Химические свойства
Для ртути характерны две степени окисления: +1 и +2. В степени окисления +1 ртуть представляет собой двухъядерный катион Hg 22+ со связью металл-металл. Ртуть – один из немногих металлов, способных формировать такие катионы, и у ртути они – самые устойчивые.
В степени окисления +1 ртуть склонна к диспропорционированию. Оно протекает при нагревании и под щ елачивании.
добавлении лигандов, стабилизирующих степень окисления ртути +2.
Из-за диспропорционирования и гидролиза гидроксид ртути ( I ) получить не удаётся.
На холоде ртуть +2 и металлическая ртуть, наоборот, сопропорционируют. Поэтому, в частности, при реакции нитрата ртути ( II ) со ртутью получается нитрат ртути ( I ).
В очень концентрированной щелочи оксид ртути частично растворяется с образованием гидроксокомплекса
Ртуть в степени окисления +2 образует уникально прочные комплексы со многими лигандами, причём как жёсткими, так и мягкими по теории ЖМКО. С йодом (-1), серой (-2) и углеродом она образует очень прочные ковалентные связи. По устойчивости связей металл-углерод ртути нет равных среди других металлов, поэтому получено огромное количество ртутьорганических соединений.
Из элементов II Б группы именно у ртути появляется возможность разрушения очень устойчивой 6 d 10 – электронной оболочки, что приводит к возможности существования соединений ртути( IV ), но они крайне малоустойчивы, поэтому эту степень окисления скорее можно отнести к курьёзной, чем к характерной. В частности, при взаимодействии атомов ртути и смеси неона и фтора при температуре 4К получен HgF 4.
Физические свойства
Плотность ртути при нормальных условиях – 13 500 кг/м3.
Таблица 1 – Зависимость плотности от температуры
Получение
Ртуть получают путём восстановления из её наиболее распространённого минерала – киновари.
Пары ртути конденсируют и собирают. Этот способ применяли ещё алхимики древности.
На протяжении многих столетий в Европе основным и единственным месторождением ртути был Альмаден в Испании. В Новое время с ним стала конкурировать Идрия вовладениях Габсбургов (современная Словения). Там же появилась первая лечебница для поражённых отравлением парами ртути рудокопов. В 2012 г. ЮНЕСКО объявило промышленную инфраструктуру Альмдена и Идрии памятником Всемирного наследия человечества.
В надписях во дворце древнеперсидских царей Ахеменидов ( VI – IV века до н. э.) в Сузах упоминается, что ртутную киноварь доставляли сюда с Зеравшанских гор и использовали в качестве краски.
Нахождение в природе
Ртуть – относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе – рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути – 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути – тиманит ( HgSe ) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.
Применение ртути и её соединений
Медицина
В связи с высокой токсичностью ртуть почти полностью вытеснена из медицинских препаратов. Её соединения (в частности, мертиолят) иногда используются в малых количествах как консервант для вакцин. Сама ртуть сохраняется в ртутных медицинских термометрах (один медицинский термометр содержит до 2 г ртути).
Однако вплоть до 1970-х годов соединения ртути использовались в медицине очень активно:
● хлорид ртути ( I ) (каломель) – слабительное;
● меркузал и промеран – сильные мочегонные;
● хлорид ртути ( II ), цианид ртути ( II ), амидохлорид ртути и жёлтый оксид ртути( II ) – антисептики (в том числе в составе мазей).
Известны случаи, когда при завороте кишок больному вливали в желудок стакан ртути. По мнению древних врачевателей, предлагавших такой метод лечения, ртуть благодаря своей тяжести и подвижности должна была пройти по кишечнику и под своим весом расправить его перекрутившиеся части.
Амальгаму серебра применяли в стоматологии в качестве материала зубных пломб до появления светоотверждаемых материалов.
Ртуть-203 ( T 1/2 = 53 сек) используется в радиофармакологии.
Техника
● Ртуть используется как рабочее тело в ртутных термометрах (особенно высокоточных), так как (а) обладает довольно широким диапазоном, в котором находится в жидком состоянии, (б) её коэффициент термического расширения почти не зависит от температуры и (в) обладает сравнительно малой теплоёмкостью. Сплав ртути с таллием используется для низкотемпературных термометров.
● Парами ртути заполняют люминесцентные лампы, поскольку пары светятся в тлеющем разряде. В спектре испускания паров ртути много ультрафиолетового света и, чтобы преобразовать его в видимый, стекло люминесцентных ламп изнутри покрывают люминофором. Без люминофора ртутные лампы являются источником жесткого ультрафиолета (254 нм), в каковом качестве и используются. Такие лампы делают из кварцевого стекла, пропускающего ультрафиолет, поэтому они называются кварцевыми.
● Ртутные электрические вентили (игнитроны) в мощных выпрямительных устройствах, электроприводах, электросварочных устройствах, тяговых и выпрямительных подстанциях и т. п. [18] со средней силой тока в сотни ампер и выпрямленным напряжением до 5 кВ.
● Ртуть и сплавы на её основе используются в герметичных выключателях, включающихся при определённом положении.
● Ртуть используется в датчиках положения.
● В некоторых химических источниках тока (например, ртутно-цинковых), в эталонных источниках напряжения (Нормальный элемент Вестона).
● Ртуть также иногда применяется в качестве рабочего тела в тяжелонагруженных гидродинамических подшипниках.
● Ртуть ранее входила в состав некоторых биоцидных красок для предотвращения обрастания корпуса судов в морской воде. Сейчас запрещается использовать такого типа покрытия.
● Иодид ртути( I ) используется как полупроводниковый детектор радиоактивного излучения.
● Фульминат ртути( II ) («гремучая ртуть») издавна применяется в качестве инициирующего ВВ (Детонаторы).
● Бромид ртути( I ) применяется при термохимическом разложении воды на водород и кислород (атомно-водородная энергетика).
● Перспективно использование ртути в сплавах с цезием в качестве высокоэффективного рабочего тела в ионных двигателях.
● До середины 20 века ртуть широко применялась в барометрах и манометрах.
● Ртутные вакуумные насосы были основными источниками вакуума в 19 и начале 20 веков.
● Ранее ртуть использовали для золочения поверхностей методом амальгамирования, однако в настоящее время от этого метода отказались из-за токсичности ртути.
● Соединения ртути использовались в шляпном производстве для выделки фетра.
Металлургия
● Металлическая ртуть применяется для получения целого ряда важнейших сплавов.
● Ранее различные амальгамы металлов, особенно золота и серебра, широко использовались в ювелирном деле, в производстве зеркал.
● Металлическая ртуть служит катодом для электролитического получения ряда активных металлов, хлора и щелочей. Сейчас вместо ртутных катодов используют электролиз с диафрагмой.
● Ртуть используется для переработки вторичного алюминия (см. амальгамация)
● Ртуть хорошо смачивает золото, поэтому ей обрабатывают золотоносные глины для выделения из них этого металла. Эта технология распространена, в частности, в Амазонии.
Химическая промышленность
● Соли ртути использовали в качестве катализатора промышленного получения ацетальдегида из ацетилена (реакция Кучерова), однако в настоящее время ацетальдегид получают прямым каталитическим окислением этана или этена.
● Реактив Несслера используется для количественного определения аммиака.
Сельское хозяйство
Высокотоксичные соединения ртути – каломель, сулему, мертиолят и другие – используют для протравливания семенного зерна и в качестве пестицидов.
Заключение
Запрет использования ртутьсодержащей продукции
С 2020 года международная конвенция, названная в честь массового отравления ртутью и подписанная многими странами, запретит производство, экспорт и импорт нескольких различных видов ртутьсодержащих продукции применяемой в быту, в том числе электрических батарей, электрических выключателей и реле, некоторых видов компактных люминесцентных ламп (КЛЛ), люминесцентных ламп с холодным катодом или с внешним электродом, ртутных термометров и приборов измерения давлении. Конвенция вводит регулирование использования ртути и ограничивает ряд промышленных процессов и отраслей, в том числе горнодобывающую (особенно непромышленную добычу золота), производство цемента.
Демеркуризация
Очистка помещений и предметов от загрязнений металлической ртутью и источников ртутных паров называется демеркуризацией. В быту широко применяется демеркуризация с помощью серы и хлорного железа FeCl 3.
Гигиеническое нормирование концентраций ртути
Предельно допустимые уровни загрязнённости металлической ртутью и её парами:
● ПДК в населённых пунктах (среднесуточная) – 0,0003 мг / м³
● ПДК в жилых помещениях (среднесуточная) – 0,0003 мг/м³
● ПДК воздуха в рабочей зоне (макс. разовая) – 0,01 мг/м³
● ПДК воздуха в рабочей зоне (среднесменная) – 0,005 мг/м³
● ПДК сточных вод (для неорганических соединений в пересчёте на двухвалентную ртуть) – 0,005 мг/ л
● ПДК водных объектов хозяйственно-питьевого и культурного водопользования, в воде водоёмов – 0,0005 мг/л
Ртуть
Ртуть — элемент побочной подгруппы второй группы, шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 80. Обозначается символом Hg (лат. Hydrargyrum). Простое вещество ртуть (CAS-номер: 7439-97-6) — переходный металл, при комнатной температуре представляет собой тяжёлую серебристо-белую заметно летучую жидкость, пары которой чрезвычайно ядовиты. Ртуть — один из двух химических элементов (и единственный металл), простые вещества которых при нормальных условиях находятся в жидком агрегатном состоянии (второй элемент — бром). В природе находится как в самородном виде, так и образует ряд минералов. Чаще всего ртуть получают путём восстановления из её наиболее распространённого минерала — киновари. Применяется для изготовления измерительных приборов, вакуумных насосов, источников света и в других областях науки и техники.
В XIX веке врачи лечили ртутью раны и венерические болезни.
Происхождение названия
Русское название ртути, по одной из версий, — это заимствование из арабского (через тюркские языки); по другой версии, «ртуть» связана с литовским ritu — качу, катаю, происшедшим от индоевропейского рет (х) — бежать, катиться.
Соединения ртути
Ртуть и её соединения применяются в технике, химической промышленности, медицине. Желтый оксид ртути (II) входит в состав глазной мази и мазей для лечения кожных заболеваний. Красный оксид ртути (II) применяется для получения красок.
Хлорид ртути (I), который называется каломель, используется в пиротехнике, а также в качестве фунгицида.
В ряде стран каломель используется в качестве слабительного. Токсическое действие каломели проявляется особенно тогда, когда после приема её внутрь не наступает слабительное действие и организм долгое время не освобождается от этого препарата. Хлорид ртути (II), который называется сулема, является очень токсичным. Сулема применялась в медицине как дезинфицирующее средство, в технике она используется для обработки дерева, получения некоторых видов чернил, травления и чернения стали.
В сельском хозяйстве сулема применяется как фунгицид. Амидохлорид ртути (белый преципитат ртути) входит в состав некоторых мазей. В ветеринарии амидохлорид ртути применяется как средство против паразитарных заболеваний кожи. Нитрат ртути (II) применяется для отделки меха и получения других соединений этого металла. Токсичность нитрата ртути (II) примерно такая же, как и токсичность сулемы. Многие органические соединения ртути используются в качестве пестицидов и средств для обработки семян. Отдельные органические соединения ртути применяются как диуретические средства.
Распространённость в природе
Ртуть относительно редкий элемент в Земной коре со средней концентрацией 0.08 частей на миллион. Однако в виду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2.5 % ртути. Иногда ртуть даже встречается в самородном виде.
В окружающей среде
До индустриальной революции осаждение ртути из атмосферы составляло около 4 нанограмма на литр льда. Природные источники, такие как вулканы, составляют примерно половину всех выбросов атмосферной ртути. За оставшуюся половину ответственна деятельность человека. В ней основную долю составляют выбросы в результате сгорания угля главным образом в тепловых электростанциях — 65 %, добыча золота — 11 %, выплавка цветных металлов — 6.8 %, производство цемента — 6.4 %, утилизация мусора — 3 %, производство соды — 3 %, чугуна и стали — 1.4 %, ртути (в основном для батареек) — 1.1 %, остальное — 2 %.
Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что привело к более чем трём тысячам жертв, которые либо умерли, либо сильно пострадали от болезни Минамата.
Получение
Ртуть получают сжиганием киновари (Сульфида ртути (II)). Этот способ применяли алхимики древности. Уравнение реакции горения киновари: HgS+O2→Hg+SO2
В России известны 23 месторождения ртути, промышленные запасы составляют 15,6 тыс.тонн (на 2002 год).
Физические свойства
Химические свойства
Ртуть — малоактивный металл (см. ряд напряжений).
При нагревании до 300 °C ртуть вступает в реакцию с кислородом: 2Hg + O2 → 2HgO Образуется оксид ртути(II) красного цвета. Эта реакция обратима: при нагревании выше 340 °C оксид разлагается до простых веществ. Реакция разложения оксида ртути исторически является одним из первых способов получения кислорода.
При нагревании ртути с серой образуется сульфид ртути(II).
Ртуть не растворяется в растворах кислот, не обладающих окислительными свойствами, но растворяется в царской водке и азотной кислоте, образуя соли двухвалентной ртути. При растворении избытка ртути в азотной кислоте на холоде образуется нитрат Hg2(NO3)2.
Из элементов IIБ группы именно у ртути появляется возможность разрушения очень устойчивой 6d 10 — электронной оболочки, что приводит к возможности существования соединений ртути (+4). Так, кроме малорастворимого Hg2F2 и разлагающегося водой HgF2 существует и HgF4, получаемый при взаимодействии атомов ртути и смеси неона и фтора при температуре 4К.
Применение
Ртуть применяется в изготовлении термометров, парами ртути наполняются ртутно-кварцевые и люминесцентные лампы. Ртутные контакты служат датчиками положения. Кроме того, металлическая ртуть применяется для получения целого ряда важнейших сплавов.
Ранее различные амальгамы металлов, особенно амальгамы золота и серебра, широко использовались в ювелирном деле, в производстве зеркал и зубных пломб. В технике ртуть широко применялась для барометров и манометров. Соединения ртути использовались как антисептик (сулема), слабительное (каломель), в шляпном производстве и т.д., но в связи с её высокой токсичностью к концу XX века были практически вытеснены из этих сфер (замена амальгамирования на напыление и электроосаждение металлов, полимерные пломбы в стоматологии).
Сплав ртути с таллием используется для низкотемпературных термометров.
Металлическая ртуть служит катодом для электролитического получения ряда активных металлов, хлора и щелочей, в некоторых химических источниках тока (например, ртутно-цинковых — тип РЦ), в эталонных источниках напряжения (Вестона элемент). Ртутно-цинковый элемент (эдс 1,35 Вольт) обладает очень высокой энергией по объёму и массе (130 Вт/час/кг, 550 Вт/час/дм).
Ртуть используется для переработки вторичного алюминия и добычи золота (см. амальгамная металлургия).
Ртуть используется в качестве балласта в подводных лодках и регулирования крена и дифферента некоторых аппаратов. [источник не указан 236 дней] Перспективно использование ртути в сплавах с цезием в качестве высокоэффективного рабочего тела в ионных двигателях.
Ртуть входит в состав некоторых биоцидных красок для предотвращения обрастания корпуса судов в морской воде.
Ртуть-203 (T1/2 = 53 сек) используется в радиофармакологии.
Также используются и соли ртути:
Иодид ртути используется как полупроводниковый детектор радиоактивного излучения.
Фульминат ртути («Гремучая ртуть») издавна применяется в качестве инициирующего ВВ (Детонаторы).
Бромид ртути применяется при термохимическом разложении воды на водород и кислород (атомно-водородная энергетика).
Некоторые соединения ртути применяются как лекарства (например, мертиолят для консервации вакцин), но в основном из-за токсичности ртуть была вытеснена из медицины (сулема, оксицианид ртути — антисептики, каломель — слабительное и др.) в середине-конце XX века.
Токсикология ртути
Пары́ ртути, а также металлическая ртуть очень ядовиты, могут вызвать тяжёлое отравление. Ртуть и её соединения (сулема, каломель, цианид ртути) поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании — дыхательные пути (а проникновение ртути в организм чаще происходит именно при вдыхании её паров, не имеющих запаха). По классу опасности ртуть относится к первому классу (чрезвычайно опасное химическое вещество). Опасный загрязнитель окружающей среды, особенно опасны выбросы в воду, поскольку в результате деятельности населяющих дно микроорганизмов происходит образованием растворимой в воде и токсичной метилртути.
Подробнее смотрите статью отравление ртутью.